நம்மைச்சுற்றி நிகழும் மாற்றங்கள் Notes 7th Science Lesson 9 Notes in Tamil
7th Science Lesson 9 Notes in Tamil
9] நம்மைச்சுற்றி நிகழும் மாற்றங்கள்
அறிமுகம்:
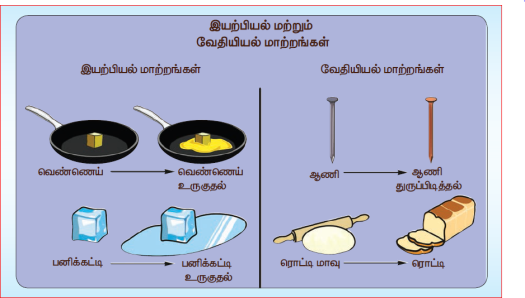
நம்மைச் சுற்றி எல்லா நேரங்களிலும் மாற்றங்கள் தொடர்ந்து நிகழ்ந்து வருகிறது. மாற்றம் என்பது ஒரு பொருளின் இயற்பியல் பண்புகளில் ஏற்படும் மாற்றமாகவோ அல்லது அப்பொருளின் வேதிப்பண்புகளில் இயைபில் ஏற்படும் மாற்றமாகவோ இருக்கும். எடுத்துக்காட்டாக, வெப்பப்படுத்தும் பொழுது பனிக்கட்டி உருகுகிறது; இதில் திண்ம நிலை பனிக்கட்டி திரவ நிலைக்கு மாறுகிறது. இம்மாற்றம் பொருளின் இயற்பியல் நிலையில் ஏற்படும் மாற்றமாகும். மற்றொரு எடுத்துக்காட்டினைக் காண்போம். அதாவது, இரும்பாலான பொருள்களை ஈரப்பதமான இடங்களில் வைக்கும்பொழுது, அப்பொருள்களின் மேல் புதிய செம்பழுப்பு நிற பொருள்கள் உருவாகியிருப்பதைக் காண்போம். இம்மாற்றத்தில் துரு என்ற புதிய பொருள் உருவானதால், இரும்பு பொருள்கள் நிறம், அமைப்பு மற்றும் நிலை ஆகியவற்றில் மாற்றம் அடைந்துள்ளது அல்லவா?
வேறு சில எடுத்துக்காட்டுகளைக் காண்போம். ஒரு குவளை நீரினையும், ஒரு தாளினையும் வெப்பப்படுத்தவும். நீரினை வெப்பப்படுத்தும் பொழுது அது மேலும் மேலும் சூடாகி, ஒரு குறிப்பிட்ட நேரத்தில் நீராவியாக மாறுகிறது. எனினும், அது நீர் என்ற பொருளாகவே திரவ நிலையிலும், வாயு நிலையிலும் இருக்கின்றது. இவ்வாறாக புதிய பொருள் எதனையும் உருவாக்கமால், நீரின் பருமனில் மட்டும் மாற்றம் ஏற்படுவது இயற்பியல் மாற்றமாகும். ஆனால் எரிக்கும்பொழுது, காகிதம் கார்பன் டைஆக்ஸைடாகவும் வேறு சில பொருள்களாவும் மாறுகிறது. இனி அந்த காகிதத்தை மீண்டும் பெற இயலாது. இவ்வாறாக, பொருளின் வேதியியல் இயைபில் ஏற்படும் மாற்றம் வேதியியல் மாற்றமாகும்.
நீங்கள் நீரில் சிறிதளவு சர்க்கரையைக் கரைத்தீர்கள் எனில், அது இயற்பியல் மாற்றமா? அல்லது வேதியியல் மாற்றமா?
பின்வரும் பட்டியலைக் காண்க. அதில் குறிப்பிட்டுள்ளவை இயற்பியல் மாற்றமா அல்லது வேதியியல் மாற்றமா என இனங்கண்டு அவற்றை கொடுக்கப்பட்டுள்ள அட்டவணையில் நிரப்புக.

(இரும்பு துருப்பிடித்தல், உணவு செரித்தல், முட்டை வேகவைத்தல், வாழைப்பழம் அழுகுதல், மணலினையும் நீரினையும் கலத்தல், மரக்கட்டையினை வெட்டுதல், தகரம் நசுங்குதல், வண்ண பட்டன்கள், கட்டை எரிதல்)
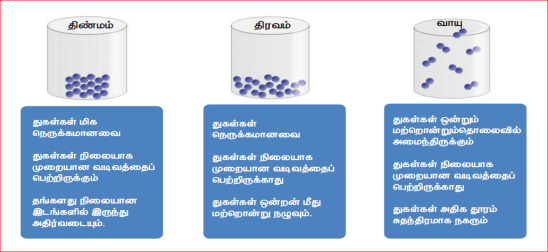
இயற்பியல் நிலையின் அடிப்படையில் பருப்பொருள்கள் திண்மம், திரவம் மற்றும் வாயு என மூன்று வகையாக வகைப்படுத்தப்பட்டுள்ளதை நாம் ஆறாம் வகுப்பில் படித்தது நினைவிலிருக்கலாம். பருப்பொருள்கள் சிறு துகள்களால் ஆனது என்றும், துகள்கள் தொடர்ச்சியாக ஒழுங்கற்ற இயக்கத்தில் ஈடுபட்டு வரும் என்பதையும் நாம் அறிவோம். திண்மம், திரவம் மற்றும் வாயுக்களின் பண்புகளை தற்போது சுருக்கமாகப் பார்ப்போமா?
அழுத்தம் கொடுத்தல், வெப்பப்படுத்துதல் போன்ற காரணங்களினாலோ அல்லது வேறு காரணங்களினாலோ ஒரு பொருளில் அமைந்துள்ள துகள்களின் அமைப்பு மாறுபடுவது என்பது அந்தப் பொருள் இயற்பியல் மாற்றம் அடைவதாகும். பொருள்களை வெப்பப்படுத்துவதால் ஏற்படும் விளைவுகளை தற்போது பார்ப்போம்.
திண்மம், திரவம், வாயுக்களின் மீது வெப்பத்தின் விளைவு:
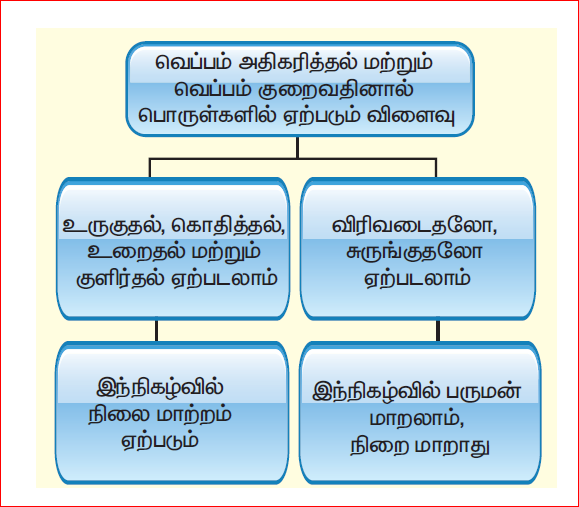
பொருள்களை வெப்பப்படுத்தும்பொழுது அதில் உள்ள துகள்களின் அமைப்பு பாதிப்படையும். அந்த பாதிப்பானது விரிவடைவதாகவோ சுருங்குதலாகவோ நம் பார்வைக்குத் தெரியும். ஒரு பொருளை வெப்பப்படுத்துவதாலோ அல்லது அப்பொருள் குளிர்விப்பதாலோ, அப்பொருளானது விரியும் அல்லது சுருங்குமேயன்றி, அந்தப் பொருளின் நிறையில் எந்த மாற்றமும் அடைவதில்லை. அதாவது, அப்பொருளில் அடங்கியுள்ள துகள்களின் எண்ணிக்கையில் எந்த மாற்றமும் ஏற்படுவதில்லை. ஆனால் அத்துகள்களின் அமைப்பில் மாற்றம் ஏற்படுகிறது. ஒரு குவளை நீரினை வெப்பப்படுத்தும்பொழுது அதன் பருமன் அதிகரிக்கிறது. மாறாக அதே குவளை நீரினை குளிர்விக்கும் பொழுது அதன் பருமன் குறைகிறது.
இவ்வாறாக பருமன் மாறுபாடு அடைந்தும், நிறை மாறாமலும் பொருள்களில் ஏற்படும் மாற்றங்களுக்கு இயற்பியல் மாற்றங்கள் என்று பெயர். இயற்பியல் மாற்றங்களை பின்வரும் படத்தில் அறியலாம்.
திண்மம், திரவம் மற்றும் வாயுக்களை வெப்பப்படுத்தும்பொழுது சுருங்குதல், விரிதலையும் கடந்து வேறு சில சாத்தியக்கூறுகள் உண்டு. உருகுதல், கொதித்தல், உறைதல் மற்றும் குளிர்வித்தல் போன்ற செயல்களால் பொருளின் இயற்பியல் நிலையில் மாற்றம் ஏற்படும். அவற்றைப் பற்றி விரிவாக பார்க்கலாம்.
இயற்பியல் மாற்றங்கள்:
ஒரு பொருளின் வேதியியல் இயைபில் எந்தவொரு மாற்றத்தையும் நிகழ்த்தாமல் அப்பொருளின் இயற்பியல் பண்புகளில் மட்டுமே ஏற்படும் மாற்றங்களுக்கு இயற்பியல் மாற்றங்கள் என்று பெயர். இயற்பியல் மாற்றத்தில் புதிய பொருள் எதுவும் உண்டாவதில்லை.

பளபளப்பு, தகடாகும் தன்மை (நெகிழ்வுத்தன்மை) மற்றும் மெல்லிய கம்பிகளாக இழுக்கக்கூடிய பண்பு, (நீளுமை) அடர்த்தி, பாகுத்தன்மை, கரைதிறன், நிறை, பருமன் போன்றவை இயற்பியல் பண்புகளுள் சில. (இயற்பியல் மாற்றங்களில் புதிய பொருள் ஏதும் உருவாவதில்லை). எடுத்துக்காட்டாக, .ஒரு இரப்பர் வளையத்தை இழுக்கும் பொழுது அது நீட்சியடைகிறது. எனினும், வளையத்தை இழுப்பதை நிறுத்திய பின்னர், அது தன்னுடைய ஆரம்ப நிலை வடிவத்திற்கு மீண்டும் வந்தடையும். இம்மாற்றத்தில் அதே இரப்பர் வளையம் இழுபட்டு மீண்டும் பழைய நிலையை எட்டுவதைத் தவிர வேறு புதிய பொருள் ஏதும் உருவாவதில்லை.
இயற்பியல் மாற்றத்தின் பண்புகள்:
ஒரு இயற்பியல் மாற்றத்தின் பண்புகள் பின்வருமாறு:
- இயற்பியல் மாற்றத்தில், புதிய பொருள்கள் ஏதும் உருவாவதில்லை. இயற்பியல் மாற்றத்தால் பொருளின் வேதியியல் இயைபில் ஏதும் மாற்றம் நிகழ்வதில்லை. எடுத்துக்காட்டாக பனிக்கட்டி உருகும் பொழுது நீர் உருவாகிறது. இம்மாற்றத்தில் பனிக்கட்டியிலும் நீரிலும் காணப்படுவது ஒரே பொருளேயன்றி வேறு வேறு பொருள் அல்ல.
- ஒரு இயற்பியல் மாற்றம் என்பது பொதுவாக தற்காலிகமானதும், மீள்தன்மை கொண்டதுமாகும். எடுத்துக்காட்டாக, நீரினை வெப்பப்படுத்தினால், நீராவி கிடைக்கிறது. கிடைத்த நீராவியை குளிரவைக்கும் பொழுது மீண்டும் அதே நீரினைத் திரும்பப் பெற இயலும்.
- இயற்பியல் மாற்றத்தில் பொருளின் வேதியியல் பண்புகளில் எந்த மாற்றமும் நிகழ்வதில்லை. எடுத்துக்காட்டாக, ஒரு தங்கத்துண்டு ஒன்றினை உருக்கும்பொழுது, திண்ம நிலை தங்கம் மற்றும் திரவ நிலைத் தங்கம் இரண்டிலும் ஒரே வேதியியல் இயைபினைத் கொண்ட தங்கத்துகள்களே காணப்படுகிறது.
இயற்பியல் மாற்றத்தில் பொருளின் வண்ணம், வடிவம், அளவுகளில் மாற்றம் நிகழலாம். எடுத்துக்காட்டாக, காய்கறிகள் வெட்டுதல் மற்றும் பலூன் ஊதுதல் போன்ற சில இயற்பியல் மாற்றங்களில் பொருளின் வடிவம் மற்றும் அளவுகளில் மட்டுமே மாற்றம் ஏற்பட்டுள்ளதை நாம் அறிவோம் அல்லவா?

நிலை மாற்றம்:
அன்றாட வாழ்வில் நாம் காணும் நிலைமாற்றம் என்பது அப்பொருளின் இயற்பியல் மாற்றங்களுள் முக்கிமானதொன்றாகும். பனிக்கட்டி உருகுதல் போன்ற எளிய இயற்பியல் மாற்றத்தில் ஏற்படும் நிலை மாற்றத்தினை முந்தைய வகுப்புகளில் படித்தது நினைவிருக்கலாம்.
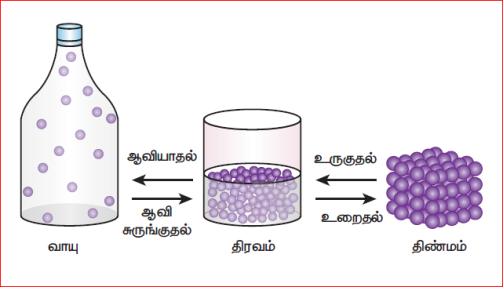
சில நிலை மாற்றங்கள் பின்வருமாறு:
| உருகுதல் | திண்மத்திலிருந்து திரவத்திற்கு மாறுவது |
| ஆவியாதல் | திரவத்திலிருந்து வாயுவிற்கு மாறுவது |
| உறைதல் | திரவத்திலிருந்து திண்மத்திற்கு மாறுவது |
| ஆவி சுருங்குதல் | வாயுவிலிருந்து திரவத்திற்கு மாறுவது |
| பதங்கமாதல் | திண்மத்திலிருந்து வாயுவிற்கு மாறுவது |
உருகுதல், ஆவியாதல் மற்றும் பதங்கமாதல் போன்றவை நிகழ வெப்பம் செலுத்தப்படுவதால் இவை வெப்பக் கொள் நிகழ்வுகளாகும். ஒரு வெப்பக் கொள் நிகழ்வில், மூலக்கூறுகளின் வேகம் அதிகரிப்பதால், அவை வேகமாக நகரும்.
எதிர்மறையாக, உறைதல் மற்றும் ஆவி சுருங்குதலில் வெப்பம் நீக்கப்படுவதால், மூலக்கூறுகளின் வேகம் குறைவதால் அவை மெதுவாக நகரும். இத்தகைய நிகழ்வுகள் வெப்ப உமிழ் நிகழ்வுகளாகும் அடுத்தப்பகுதியில் ஒவ்வொரு இயற்பியல் மாற்றங்களையும் பார்க்கலாம்.
உருகுதல்:
ஒரு குவளையில் உள்ள பனிக்கட்டிகளையோ அல்லது ஒரு கிண்ணத்தில் உள்ள பனிக்கூழினையோ அறை வெப்ப நிலையில் வைக்கும்பொழுது அதனைச் சுற்றி குட்டை போல் நீர் தேங்கி இருப்பதைப் பார்த்திருப்பீர்கள். பனிக்கட்டி/பனிக்கூழ் உருகுவதால் தானே! அதன் காரணத்தைக் கூற முடியுமா?
குவளையில் உள்ள பனிக்கட்டி சுற்றுப்புறத்திலுள்ள வெப்பத்தைப் பெற்று உருகி, நீராக மாறுகிறது.
இதிலிருந்து நாம்அறிவது:
வெப்பப்படுத்துதல்
திண்மம் —————————-> திரவம்
குளிர்வித்தல்
திரவம் —————————-> திண்மம்
ஒரு பொருளை வெப்பப்படுத்துதல் மூலம் திண்ம நிலையிலிருந்து திரவ நிலைக்கு மாற்றுவது உருகுதல் ஆகும். மாறாக, ஒரு பொருளை குளிர்விக்கும் போது திரவ நிலையில் இருந்து திண்ம நிலைக்கு மாற்றும் நிகழ்வு உறைதல் ஆகும்.
ஆவியாதல்:
நீர் கொண்ட ஒரு கெட்டிலைக் போதுமான அளவு வெப்பப்படுத்தியதும், நீர்க்குமிழ்கள் உருவாகி திரவ நிலை நீர், நீராவியாக மாறுவதைக் காணலாம்.
எனினும், ஈரமான ஒரு துணியினை உலர்த்தும்பொழுது துணியில் உள்ள நீர் ஆவியாகி துணியினை உலர வைக்கிறது.
ஆக, ஆவியாதல் இரு வகையில் நிகழும்: கொதித்தல் மற்றும் ஆவியாதல், கொதித்தல் வெப்பப்படுத்துதல் மூலமும், ஆவியாதல் இயற்கையிலேயே நிகழும் ஒரு நிகழ்வாகவும் அமைகிறது.
கொதித்தல், என்ற நிகழ்வில் ஒரு திரவம் வெப்பத்தினை ஏற்று அதன் வாயுநிலைக்குப் போகிறது. வாயு நிலையில் அதில் அமைந்துள்ள மூலக்கூறுகளின் அமைப்பு மட்டுமே மாற்றம் அடைகிறதேயன்றி அதில் வேறு எந்த வேதியியல் இயைபும் மாற்றம் அடைவதில்லை. ஆகையால் கொதித்தல் என்பது ஒரு இயற்பியல் மாற்றமாகும்.
ஒரு திரவத்தினை வெப்பப்படுத்தும்பொழுது, அதன் துகள்கள் அதிக ஆற்றலைப் பெற்று வேகமாக அதிர்வடைகிறது. போதிய ஆற்றலைப் பெற்றவுடன், துகள்கள் தன்னிடையே உள்ள ஈர்ப்பு விசையினைத் எதிர்கொண்டு, ஒன்றையொன்று விலக்கி தனித்தனியே ஒழுங்கற்றதா இடம்பெயர்கிறது. எடுத்துக்காட்டாக, நீரினை 1000Cக்கு வெப்பப்படுத்தும் பொழுது, அது கொதித்து நீராவியாகிறது. கொதிநிலையை அடைந்தவுடன் கொதித்தல் நடைபெறுகிறது. திரவ நிலையில் இருந்து வாயுவிலைக்கு மாறுகிறது.
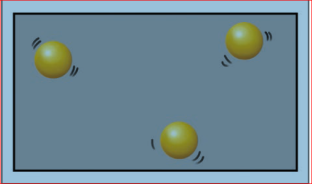
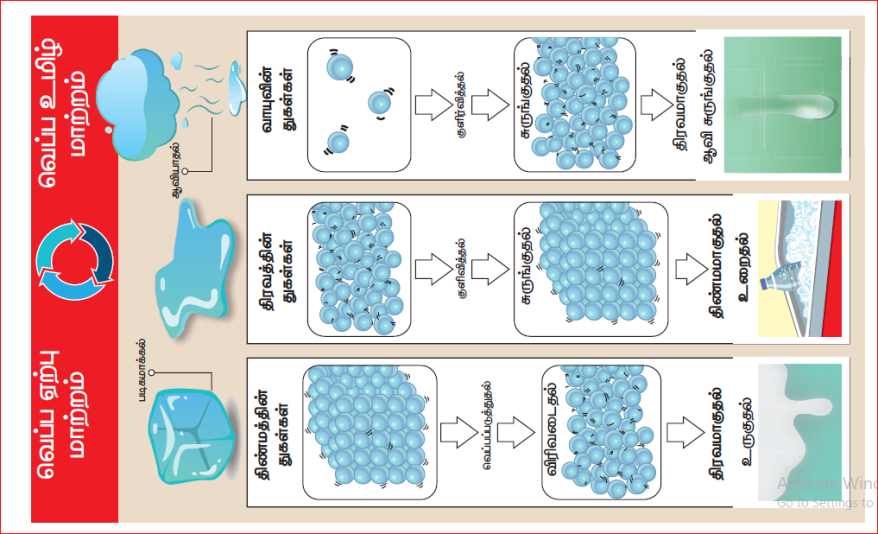
வாயுவின் துகள்கள்
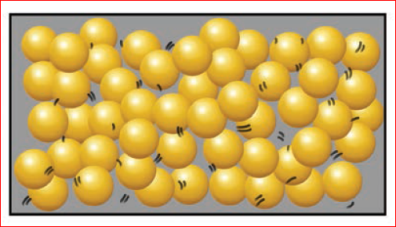
திரவத் துகள்கள்
ஆவியாதல்:
ஒரு குவளையில் நீரினை எடுத்துக் கொள்ளவும். அதில் உள்ள நீர் மூலக்கூறுகள் இங்கும் அங்கும் வெவ்வேறு திசைவேகத்தில் (படத்தில் வெவ்வேறு அளவிலான அம்புகுறிகளாக காட்டப்பட்டுள்ளது) நகர்ந்தபடி இருக்கும். சில மூலக்கூறுகள், அதிலும் குறிப்பாக நீரின் மேற்பரப்பில் உள்ள மூலக்கூறுகள் திரவத்தினை விட்டுவிலகியபடி எதிர்திசையை நோக்கி, அதாவது காற்றினை நோக்கி நகர போதிய அளவு ஆற்றலைப் பெற்று, நீரின் பரப்பு இழுவிசையினையும் தாண்டி, திரவ கலனை விட்டு ஆவியாக வெளியேறுகிறது. நேரம் ஆக ஆக, கலனில் உள்ள நீரின் அளவு தொடர்ந்து குறைந்து வருகிறது.
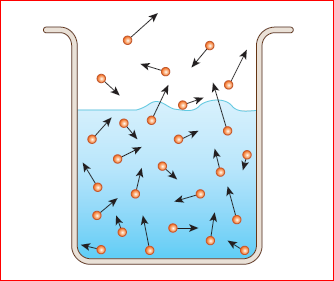
தண்ணீரின் வெப்பநிலை நீரின் கொதிநிலை அளவுக்கு உயரவில்லை என்பதை நினைவில் கொள்க. கொதிப்பது போல் எந்த நீர்க்குமிழ்களும் அங்கு தோன்றவில்லை.
ஆவியாதல் என்ற நுட்பத்தினைப் பயன்படுத்தி கரைந்த நிலையில் உள்ள திண்மங்களை அதன் திண்மம் – திரவம் கலவையில் இருந்து பிரித்தெடுக்க முடியும். இம்முறையின் மூலம் கடல் நீரினை அதிக பரப்புள்ள நிலத்தில் சிறிதளவு கடல் நீர் பரவலாக ஊற்றப்படுகிறது. இதுவே உப்பளமாகும். இவ்வாறு செய்வதால் சூரிய வெப்பத்தால் நீர் மேல் பட்டு அதிலுள்ள நீரினை மெதுவாக ஆவியாகிறது. இறுதியில் உப்பு நிலத்தில் படிகிறது. ஒரு கரைசலில் உள்ள கரைப்பான் எந்த வெப்ப நிலையிலும் அதிலுள்ள திண்மத்தை விட்டு ஆவியாகி வெளியேறும் என்ற தத்துவத்தின் அடிப்படையில் நம்மால் ஆவியாதலைப் புரிந்து கொள்ள முடியும்.
ஆவியாதல் என்ற நுட்பம் துணிகளை உலர்த்துவது முதல் மீன்களை உலர வைப்பது வரை பயனளிக்கிறது.
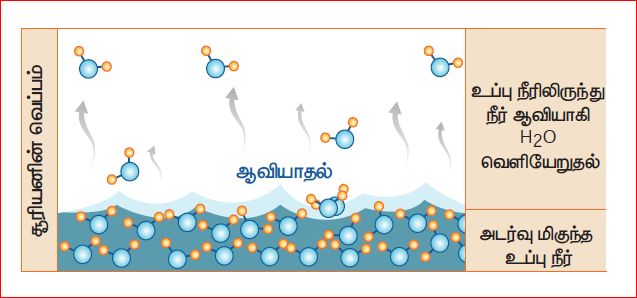
ஆவியாதலை பாதிக்கும் காரணிகள்:
ஆவியாதல் ஒரு மெதுவாக நடைபெறும் நிகழ்வு; மேலும் அது திரவத்தின் புறப்பரப்பில் மட்டுமே நிகழ்வதாகும்.
உறைதல்:
குளிர்சாதனப்பெட்டியின் அதிகுளிர் பகுதியில் வைக்கப்பட்ட நீர் மேலும் குளிர்ந்து, உறைந்து பனிக்கட்டியாக மாறுகிறது. இதில் திரவ நிலையில் இருந்த நீர், திண்ம நிலை நீராக – அதாவது பனிக்கட்டியாக மாறுகிறது.
பனிக்கட்டி உருவாகும் இந்நிகழ்வில் திரவ நிலையில் இருந்து திண்ம நிலைக்கு மாறுவதைத் தவிர வேறெந்த மாற்றமும் நிகழ்வதில்லை, வேறெந்த புதிய பொருளும் உருவாவதில்லை. எனவே, உறைதல் என்பது ஒரு இயற்பியல் மாற்றமாகும்.
ஒரு திரவத்தினை குளிர்விக்கும்பொழுது, அதன் துகள்கள் ஆற்றலை இழந்து அதனால் அதிர்வடைவதன் வேகமும் குறைகிறது. துகள்களுக்கு ஆற்றல் குறைவாக இருப்பதால் அவை ஒன்றையொன்று அதிகமாய் ஈர்த்து, நெருங்கி வர வாய்ப்புள்ளது. எனவே, அத்துகள்களின் நகர்தலும் குறைவாகவே இருக்கிறது. எடுத்துக்காட்டாக, திரவ நிலையிலுள்ள நீர் O0Cக்கு குளிர்விக்கப்படும்பொழுது, அது உறைந்து பனிக்கட்டியாகிறது. உறைநிலையை அடைந்தவுடன் அனைத்து திரவமும் உறைந்து திண்ம நிலையை அடைகிறது. திரவ நிலையிலும் திண்ம நிலையிலும் உள்ள துகள்களின் அமைப்பை பின்வரும் படத்தில் காணலாம்.
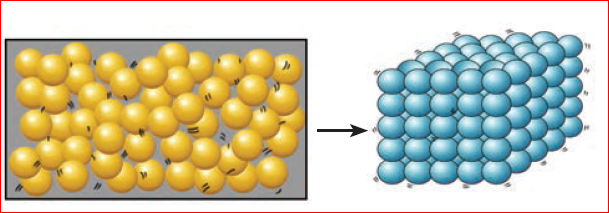
ஒரு திரவத்தின் துகள்கள் ஒரு திண்மத்தின் துகள்கள்
ஆவி சுருங்குதல்:
சமைத்த உணவுப் பதார்த்தங்களை மூடியுள்ள தட்டுக்களை அகற்றும் பொழுது அதன் உள்பகுதி முழுதும் நீர்த் திவலைகள் காணப்படுவதைப் பார்த்திருக்கிறோம் அல்லவா? அதன் காரணம் என்ன?
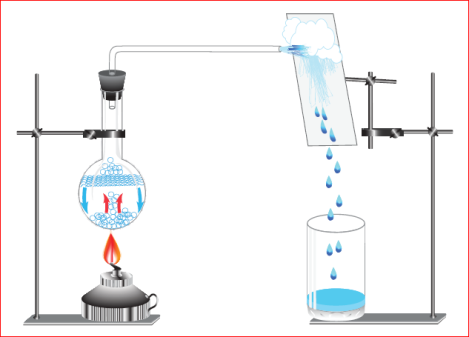
சூடான உணவில் இருந்து நீராவி வெளியேறி மேலே எழுகிறது. அவ்வுணவினை மூடிய தட்டானது சூடான உணவினை விட குறைவான வெப்பநிலையில் இருக்கிறது. அதனால் சூடான நீராவி மூலக்கூறுகள், குளிர்ந்த தட்டில் மோதும்பொழுது தனது சக்தியை இழக்கிறது; அதனால் அவற்றின் வேகமும் குறைகிறது. அதனால் நீராவி மூலக்கூறுகள் ஒன்றையொன்று ஈர்த்து, நெருங்கி வருகிறது. இறுதியாக நீராவி மூலக்கூறுகள் இணைந்து நீராகிறது. ஒரு வாயுவில் உள்ள மூலக்கூறுகள் குளிர்வடையும் பொழுது அதன் ஆவி சுருங்கி நீர்மமாகிறது.
ஆறாம் வகுப்பில் நீர் சுழற்சி பற்றி படிக்கும்பொழுது, நீராவியில் இருந்து மேகங்கள் உருவாவதைப்பற்றி படித்தது நினைவிருக்கலாம். நீராவி சுருங்கி மேகங்கள் ஆகும் அல்லவா?
வாயு நிலையினைச் சுருக்கி நீர்மமாக்கும் நிகழ்விற்கு ஆவி சுருங்குதல் என்று பெயர். ஆவி சுருங்கிய பின் கிடைக்கும் திரவத்தினை வெப்பப்படுத்தி மீண்டும் ஆவியாக மாற்ற இயலும். எனவே, ஆவி சுருங்குதல் என்ற நிகழ்வும் இயற்பியல் மாற்றமே. இந்நிகழ்வில், வாயு நிலையில் மூலக்கூறுகளின் அமைப்பு – வேறு மாதிரியும், திரவ நிலையில் உள்ள மூலக்கூறுகளின் அமைப்பு வேறு மாதிரியும் இருக்கும். எனவே, ஆவி சுருங்குதலும் ஒரு இயற்பியல் மாற்றமே.
குளிர்வித்தல்
வாயு —————————> திரவம்
வெப்பப்படுத்துதல்
திரவம் —————————> வாயு
ஒரு வாயுவினை குளிர்வித்து நீர்மமாக்கும் நிகழ்விற்கு ஆவி சுருங்குதல் என்று பெயர். ஒரு திரவத்தினை வாயு நிலைக்கு வெப்பப்படுத்துவதன் மூலம் மாற்றும் நிகழ்விற்கு ஆவியாதல் என்று பெயர்.
பதங்கமாதல்:
சில வீடுகளில் கற்பூரம் ஏற்றி வைப்பதை பார்த்திருப்பீர்கள், சில வீடுகளில் கொசுக்கள் வராமல் இருப்பதற்கு கற்பூரம் வைக்கப்பட்டிருப்பதைப் பார்த்திருப்பீர்கள். எப்பொழுதாவது கற்பூரம் உருகி திரவமானதைப் பார்த்திருக்கிறீர்களா?
அவ்வாறு நிகழ்வதில்லை அல்லவா?
கற்பூரம், நாப்தலீன் போன்ற சில திண்மப் பொருள்களை வெப்பப்படுத்தும்பொழுது திரவ நிலைக்கு மாறாமல், நேரிடையாக வாயு நிலைக்கு மாறுகிறது. இவ்வாறாக திண்ம நிலையில் இருந்து வாயு நிலைக்கு பொருள்கள் மாறும் நிகழ்விற்கு பதங்கமாதல் என்று பெயர்.
மேற்சொன்ன அனைத்து முறைகளிலும், வெப்ப நிலையை மாற்றும்பொழுது பொருள்களின் நிலையில்மாற்றம் ஏற்படுகிறது. ஆனால் அப்பொருள்களின் வேதியியல் இயைபில் எந்த மாற்றமும் நிகழவில்லை. வெப்ப நிலையை மாற்றும்போது இவ்வணைத்து மாற்றங்களையும் மீள செய்ய முடியும் பொருள்களின் இயற்பியல் நிலைமாற்றம் என்பது இயற்பியல் மாற்றமே என்று நாம் அறிவோம். ஆகையால், ஆவியாதல், கொதித்தல், ஆவி சுருங்குதல், உருகுதல் மற்றும் உறைதல் ஆகியவை இயற்பியல் நிகழ்வுகளே. எனவே, இவை அனைத்தும் இயற்பியல் மாற்றங்களே.
படிகமாக்குதல்:
முன்பே குறிப்பிடவில்லையெனினும், படிகமாக்குதல் என்பதும் ஒரு விதமான இயற்பியல் மாற்றமே. படிகமாக்குதல் மூலம் கரைந்த நிலையில் உள்ள மாசுக்களை நீக்க முடியும். ஒரு சூடான செறிந்த கரைசலில் இருந்து படிகங்களைப் பெறும் முறைக்கு படிகமாக்குதல் என்று பெயர்.
கடல் நீரில் உப்புகள் கரைந்த நிலையில் இருப்பதையும் அவற்றை ஆவியாதல் மூலம் தூய்மைப்படுத்தலாம் என்பதையும் நாம் அறிவோம். எனினும், ஆவியாதல் என்ற நிகழ்வு சிறந்த தூய்மைப்படுத்தும் முறை என்று சொல்வதற்கில்லை. ஏனெனில் கரைந்தநிலை மாசுக்களை ஆவியாதல் மூலம் நீக்க முடியும். மேலும், ஆவியாதல் மூலம் பெறப்படும் படிகங்கள் அளவில் சிறியதாக இருக்கும். படிகங்களின் வடிவத்தையும் தெளிவாகப் பார்க்க இயலாது. எனவே, திண்மப் பொருள்களை படிகமாக்குதல் மூலம் தூய்மைப்படுத்தலாம். பெரிய படிகங்களை அதன் கரைசல்களில் இருந்து பெறவும் முடியும். படிகமாக்குதல் என்பது ஒரு பிரித்தெடுக்கும் முறையாகவும் தூய்மையாக்கும் முறையாகவும் திகழ்கிறது.
வேதியியல் மாற்றங்கள்:
மாறுபட்ட வேதியியல் இயைபுடன் புதிய பொருள் உருவாவதோடு, வெப்பமோ, ஒளியோ வெளியிடப்பட்டோ அல்லது பொருள் வேறு பொருளாக மாறுவதே வேதியியல் மாற்றங்கள் எனப்படும். இரும்பு துருப்பிடித்தல், பால் தயிராதல், எலுமிச்சைச் சாறுடன் சமையல் சோடா ஈடுபடும் வினை, நொதித்தல் போன்ற செயல்கள் வேதியியல் மாற்றங்களுக்கு எடுத்துக்காட்டுகளாகும்.
நம் வாழ்வில் வேதியியல் மாற்றங்கள் மிக முக்கியமானதாகும். நம் அன்றாட வாழ்வில் நாம் பயன்படுத்தும் பெரும்பாலான பொருள்கள் வேதியியல் மாற்றங்களால் உருவானவையே வேதயியல் மாற்றங்களின் முக்கியத்துவத்தினை எடுத்துரைக்கும் விதமாக பின்வரும் சில பயன்களைக் காணலாம்.
- இயற்கையில் காணப்படும் தாது உப்புகளில் இருந்து பல தொடர்ச்சியான வேதியியல் மாற்றங்களால் உலோகங்கள் பிரித்தெடுக்கப்படுகின்றன.
- தொடர்ச்சியான பல வேதியியல் மாற்றங்களினால் மருந்துகள் தயாரிக்கப்படுகின்றன.
- பல்வேறு வகையான வேதியியல் மாற்றங்களினால் ப்ளாஸ்டிக்குகள், சோப்புகள், சலவைக்கட்டிகள், வாசனைத் திரவியங்கள், அமிலங்கள், காரங்கள், உப்புகள் மற்றும் இன்ன பிற பொருள்கள் போன்றவை தயாரிக்கப்படுகின்றன.
- பல்வேறு வகையான வேதியியல் மாற்றங்களை ஆராய்ச்சி செய்வதன் மூலம் ஒவ்வொரு புதிய பொருளும் கண்டுபிடிக்கப்படுகிறது.
புதிய பொருள்கள் உருவாவதுடன், வேறு சில நிகழ்வுகளும் ஒரு வேதியியல் மாற்றத்தின் பொழுது நிகழ்கின்றன.
- வெப்பம், ஒளி அல்லது வேறு ஏதேனும் கதிர்வீச்சு வெளியிடப்படலாம்.
- ஒலி உண்டாகலாம்.
- வீசும் மணத்தில் மாற்றமோ அல்லது புதிய மணம் உருவாவதோ நிகழலாம்.
- நிற மாற்றம் ஏற்படலாம்.
- ஏதேனும் வாயு உருவாக்கலாம்.
பட்டாசு வெடித்தல் வேதியியல் மாற்றமாகும். பட்டாசு வெடிக்கும் பொழுது வெப்பம், ஒளி, ஒலி மற்றும் விரும்பத்தகாத வாயுக்கள் வெளியிடப்பட்டு சுற்றுச்சூழலை மாசுபடுத்தும் என்பது நாமறிந்ததே. அதனால் தான் நம்மை பட்டாசுகளுடன் விளையாட வேண்டாம் என்று அறிவுறுத்தப்படுகிறது.
நறுக்கிய ஆப்பிள் துண்டுகளை நாம் உடனடியாக உண்ணாமல் வைத்திருந்தால் அவை பழுப்புநிறமாக மாறிவிடுவதை கவனித்திருப்பீர்கள்,
தோல் நீக்கி நீரில் வைக்கப்பட்ட உருளைக்கிழங்கு அதே வெண்மை நிறத்தில் உள்ளதையும், மாறாக, தோல் நீக்கி காற்றில் வைக்கப்பட்ட உருளைக்கிழங்கு நிறம் மங்கியிருப்பதையும், வெட்டி வைக்கப்பட்ட கத்திரிக்காய் நிறம் மாறியிருப்பதையும் காண்கிறாய் அல்லவா? புதிய பொருள்கள் உருவாவதால் இத்தகைய நிற மாற்றங்கள் ஏற்படுகின்றன. இவற்றைப் பற்றி உயர் வகுப்புகளின் படிக்க இருக்கிறீர்கள். இவை அனைத்தும் வேதியியல் மாற்றங்கள் எனக் கொள்ளலாம்.
இரும்பு துருப்பிடித்தல்:
இரும்பு துருப்பிடித்தல் வேதியியல் மாற்றத்திற்கான எடுத்துக்காட்டு என ஆறாம் வகுப்பில் படித்திருக்கிறோம் அல்லவா? தற்பொழுது, இரும்பு துருப்பிடித்தல் எவ்வாறு வேதியியல் மாற்றம் என்ற காரணத்தை அறிவோமா?
துருப்பிடித்தல் என்ற மாற்றம் இரும்புப் பொருள்களை பாதிப்படையச் செய்து நாளடைவில் அவற்றை மெல்ல அழித்து விடும். பாலங்கள், கப்பல்கள், கார்கள், லாரியின் பாகங்கள் போன்ற பல உறுதியான பொருள்கள் இரும்பினால் செய்யப்படுவதால், அவை துருப்பிடித்து வீணானால், பெருமளவில் பண இழப்பு ஏற்படும். கீழ்காண்பது துரு உருவாகும் முறையாகும்:
இரும்பு + ஆக்ஸிஜன் + நீர் ???? துரு
Fe + 3O2 + 2H2O ???? 2Fe2O3.H2O
இரும்பு துருப்பிடிக்க ஆக்ஸிஜன் மற்றும் நீர் இரண்டும் (அல்லது) ஈரப்பதம் மட்டுமே போதுமானது ஒரு வேளை காற்றில் ஈரப்பதம் அதிகமாக இருப்பின், துருப்பிடித்தலும் விதைவாகவே நடக்கும்.
துருப்பிடித்தலை எவ்வாறு தடுக்கலாம்?
இரும்பினால் செய்யப்பட்ட பொருள்கள் ஆக்ஸிஜன், நீர், நீராவியுடன் தொடர்புறாதாவாறு கவனித்துக் கொள்ள வேண்டும். இரும்புப் பொருள்களின் மீது மெல்லிய படலமாக பெயிண்டையோ அல்லது கிரீஸையோ பூசுவது எளிய முறையாகும். இத்தகைய படலங்களை அவ்வப்பொழுது பூசுவது துருப்பிடித்தலைத் தடுக்கும்.
எரிதல்:
காகிதம் எரிதல் வேகமாக நிகழும் மாற்றத்திற்கு எடுத்துக்காட்டு ஆகும். ஒரு காகிதத்தினை எரிய வைக்கும் பொழுது, அதிலிருந்து கார்பன் டை ஆக்ஸைடு, நீர், நீராவி, புகை, சாம்பல் போன்றவை பெறப்படுகிறது. இந்த பொருள்களை இணைத்து மீண்டும் காகிதத்தைப் பெறுதல் இயலாது. எனவே, இது ஒரு நிலையான மாற்றமாகும். தற்பொழுது, மக்னீசியம் நாடாதுண்டு ஒன்றினை எரியவைத்து அந்நிகழ்வு எந்த வகையான மாற்றம் என வகைப்படுத்தலாமா?
நீங்கள் என்ன காண்கிறீர்கள்?
திகைப்பூட்டும் வெண்ணிற ஒளியில் மெக்னீசியம் நாடா எரிவதைக் காணலாம். எரியும் மெக்னீசியம் நாடாவினை ஒரு கண்ணாடித் தட்டில் நீட்டினால், வெண்ணிற தூளாக சாம்பலைச் சேகரிக்க முடியும்.
காற்றில் மெக்னீசியம் நாடா எரியும் பொழுது, மெக்னீசியம் நாடா ஆக்ஸிஜனுடன் இணைந்து மெக்னீசியம் ஆக்ஸைடு என்ற புதிய பொருள் ஒன்று உருவாகிறது.
மக்னீசியம் + ஆக்ஸிஜன் ???? மெக்னீசியம் ஆக்ஸைடு
2Mg + O2 ???? 2MgO
மெக்னீசியம் ஆக்ஸைடு என்ற சேர்மம் வெண்ணிற சாம்பல் தூள் போல் காணப்படுகிறது. மெக்னீசியம் நாடா ஆக்ஸிஜனுடன் இணையும் நிகழ்வில் மெக்னீசியம் ஆக்ஸைடு என்ற புதிய பொருள் ஒன்று உருவாவதால் இது வேதியியல் மாற்றமாகும்.
பால் தயிராதல்:
பால் தயிராதல் என்பது மீளா வினைக்கான எடுத்துக்காட்டு என்பதை நாம் அறிவோம், ஏனெனில் தயிரான பின் எம்முறையிலும் மீண்டும் பாலினைப் பெற முடியாது. இது ஒரு வேதியியல் மாற்றமாகும். பால் தயிராகும் நிகழ்வினை மேலும் அறிவோமா?
தயிராதல் என்ற நிகழ்வில் திரவ நிலை பாலானது படிப்படியாக அதன் துகள்கள் இணைந்து கூழ்மநிலைப் பொருளாகச் சேர்ந்து திடநிலைபோல் உருவாகிறது. ஒரு பாத்திரத்தில் சூடான பாலினை எடுத்துக்கொண்டு, அதில் சிறிதளவு தயிரினைச் சேர்க்கவும், பால் திரிதல் அடைந்து சிறுசிறு திண்ம நிலை கூழ்மங்களாக உருவாகும். சூடான பாலில் சிறிதளவு எலுமிச்சைச் சாற்றை ஊற்றியும் பாலினைத் திரிய வைக்கலாம். ஆனால் அவ்வாறு திரிதல் அடைந்து பெற்ற தயிரின் சுவையும், தன்மையும் சில மணி நேரங்களில் எடுத்துக்கொண்டு இயல்பாக, மெதுவாக உரையிட்ட தயிரைப்போல் சுவையும் நயமும் இருக்காது. உடனடித் திரிதலில் பெற்ற தயிரையும், இயல்பாக உறைந்த தயிரினையும் சுவைத்துப் பார்த்து வேறுபாடு அறியவும்.
நொதித்தல்:
இட்லி மாவு தயாரித்தல் என்பது மீளா மாற்றத்தின் எடுத்துக்காட்டு என்று ஆறாம் வகுப்பில் படித்தது உங்களுக்கு நினைவிருக்கலாம்.
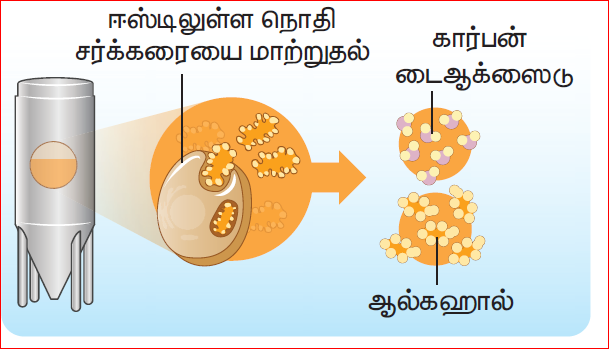
ஈஸ்ட் மற்றும் சிலவகை பாக்டீரியாக்களினால் சாக்கரைக் கரைசலினை ஆல்கஹாலாகவும், கார்பன் டை ஆக்ஸைடாகவும் மாறும் நிகழ்விற்கு நொதித்தல் என்று பெயர்.
இந்நிகழ்வினில் உண்டான ஆல்கஹாலினை மீண்டும் சர்க்கரையாக மாற்ற இயலாது. எனவே, நொதித்தல் என்பது ஒரு வேதியியல் மாற்றமாகும்.
சமையல் சோடாவும் எலுமிச்சை சாறும் இணையும் வினை:
சமையல் சோடா என்பது சோடியம் பை கார்பனேட்; எலுமிச்சைச் சாற்றில் சிட்ரிக் அமிலம் உள்ளது. இவ்விரண்டையும் கலக்கும்பொழுது, ஒரு வேதிவினை நடைபெற்று சோடியம் சிட்ரேட் என்ற உப்புடன் நீரும், கார்பன் டை ஆக்ஸைடும் வெளியேறுகிறது. இவ்வேதி வினையினை பின்வரும் வார்த்தைச் சமன்பாடாக எழுதலாம்.
சோடியம் பை கார்பனேட் + சிட்ரிக் அமிலம் ???? சோடியம் சிட்ரேட் + கார்பன் டைஆக்ஸைடு + நீர்
ஒரு வேதியியல் மாற்றம் நிகழத் தகுந்த காரணங்கள்:
பட்டாசு வெடித்தல் ஒரு வேதியியல் மாற்றமாகும். சில வகை பட்டாசுகள் சுவற்றில் அடிக்கும் பொழுதும், சில வகை பட்டாசுகளை கடினமான பொருள்களை வைத்து தட்டும்பொழுதும் வெடிக்கும். எனவே அழுத்தம் தருவதன் மூலம் ஒரு வேதியியல் மாற்றத்தினை உருவாக்கலாம் என்று காண்கிறோம்.
எலுமிச்சை சாற்றினை சோடா நீரில் ஊற்றும் பொழுது நுரைத்துப் பொங்கி கார்பன் டை ஆக்ஸைடு உருவாவதைக் காண்கிறோம். இரு கரைசலும் கலக்கும் முன் நுரைத்துப் பொங்குதல் நிகழ்வதில்லை. எனவே இரு பொருள்களின் இணைதலும் ஒரு வேதி மாற்றம் நிகழ போதுமானது என அறிகிறோம்.
வேக வைக்காத அரிசியையும், வேகவைத்த சாதத்தினையும் நாம் சுவைத்திருக்கிறோம் அல்லவா? இரண்டின் சுவையும் முற்றிலும் வெவ்வேறானவை! இந்த எடுத்துக்காட்டில், சமையல் என்ற நிகழ்வு இந்த மாற்றத்திற்கான காரணமாக உள்ளது. அரிசியுடன் தகுந்த அளவு நீரினைச் சேர்த்து, வெப்பப்படுத்தி வேகவைக்கும்பொழுது அரிசியின் தன்மையும், சுவையும் முற்றிலும் மாறிவிடுகிறது. எனவே, வெப்பப்படுத்துதல் என்ற காரணியும் ஒரு வேதி மாற்றம் நிகழ்த்த தகுந்தது என ஏற்கிறோம்.
சமையலில் வனஸ்பதியின் பயன்பாடு நாம் அறிந்ததே. தாவர எண்ணெய்களில் ஹைட்ரஜன் சேர்க்கப்பட்டு வனஸ்பதி உருவாகிறது. இவ்வினையில், நிக்கல், பிளாட்டினம் அல்லது பல்லேடியம் வினையூக்கியாகப் பயன்படுகிறது.
நீர் என்ற வேதிச் சேர்மம் எந்த காரணிக்கும் உட்படாதவரை நீராகவே இருக்கும். ஆனால், அந்நீரில் சில துளிகள் அமிலத்தினைச் சேர்த்து அதனை மின்னாற்பகுப்பிற்கு ஈடுபடுத்தினால், நீர் பிரிகை அடைந்து ஹைட்ரஜன் மற்றும் ஆக்ஸிஜன் வாயுக்களாக மாறுகிறது. இந்நிகழ்வின் மூலம் மின்சாரமும் ஒரு வேதி மாற்றம் நிகழத் தேவையான காரணி என புரிந்து கொள்ள முடியும்.
பொருள்கள், கலத்தல், வெப்பம், ஒளி, மின்சாரம், அழுத்தம் கொடுத்தல் போன்ற சில காரணிகளால் வேதி மாற்றங்களை உருவாக்க முடியும் என்று தொகுக்கலாம்.
ஒரு வேதியியல் மாற்றத்pனை சுட்டும் குறியீடுகள்:
ஒரு சோதனைக்குழாயில் சிறிதளவு தூளாக்கிய முட்டை ஒட்டுடன் எலுமிச்சைச் சாற்றினைச் சேர்க்கவும். சிறு குமிழ்களாக கார்பன் டை ஆக்ஸைடு உருவாவதைச் சோதனைக் குழாயில் காணலாம். இரு பொருள்களுக்கு இடையில் வேதி வினை நிகழ்வதை இது சுட்டுகிறது. எனவே, குமிழ்கள் வெளியேறுதல் என்ற குறியீட்டின் மூலம் அங்கு ஒரு வேதியியல் மாற்றம் நிகழ்ந்திருப்பதை அறியலாம்.
சுட்ட சுண்ணாம்புடன் (கால்சியம் ஆக்ஸைடு) நீரினைச் சேர்க்கும் பொழுது அதிகளவு வெப்பம் வெளியேறி தெளிந்த சுண்ணாம்பு (கால்சியம் ஹைட்ராக்ஸைடு) உருவாகிறது. இது ஒரு வேதியியல் மாற்றமாகும். சுட்ட சுண்ணாம்பும் நீரும் வினைபடுவதை அவை இணைதலால் உருவாகும் வெப்பத்தின் மூலம் குறிப்பாக அறிகிறோம்.
அன்றாடம் நாம் உணவுப் பதார்த்தங்கள் சமைக்கிறோம். பாத்திரங்கள் காலியானதும் அவற்றைச் சுத்தம் செய்கிறோம். ஒருவேளை மீதமான சிறிதளவு உணவுப் பதார்த்தத்துடன் பாத்திரத்தைக் கழுவாமல் மூடிய நிலையில் ஒரு நாள் விட்டுவைத்து, மறுநாள் அந்தப் பாத்திரத்தைத் திறந்தால் பாத்திரங்களில் இருந்து துர்நாற்றம் வீசுவதை உணரலாம். ஏனெனில், உணவுப் பொருள்கள் கெட்டுப்போதல் என்ற வேதிமாற்றம் அங்கு நிகழ்ந்துள்ளதால், அந்த மாற்றத்தினை துர்நாற்றத்தின் மூலம் அறிகிறோம். எனவே, மணம் மாறி துர்நாற்றமாவதும் ஒரு வேதி மாற்றத்தினைச் சுட்டும் குறியீடாகும்.
ஒரு இரும்பாலான ஆணியை சில நாள்கள் நீரில் போட்டு வைத்து, பின்னர் அதனைப் பார்க்கும் பொழுது செம்பழுப்பு நிறமாக ஒரு படலம் ஆணிமேல் இருப்பதைக் காணலாம். துருப்பிடித்தல் என்பது ஒரு வேதியியல் மாற்றம் என நாம் அறிவோம். இரும்பு ஆணியின் நிறமாற்றம் வேதி நிகழ்வினைச் சுட்டும் காரணியாகும்.
சூடான பாலில் எலுமிச்சைச் சாற்றினைக் கலந்தால் பால் திரிந்து தயிராவதை அறிவோம். தயிர் என்ற வீழ்படிவு உருவாவது என்பது சூடான பாலுக்கும் எலுமிச்சைச் சாற்றுக்கும் இடையே நிகழும் வினையினைச் சுட்டும் குறியீடாகும்.
குமிழ்கள் வெளியேறுதல், வெப்பம் வெளியிடப்படுதல், நிறமாற்றம், மண மாற்றம் அல்லது வீழ்படிவு உருவாவது போன்ற குறியீடுகள், அந்தச் சந்தர்பங்களில் ஒரு வேதி மாற்றம் நிகழ்ந்துள்ளதைச் சுட்டுகிறது எனத் தொகுத்துக் கூறலாம்.
வெப்ப ஏற்பு மற்றும் வெப்ப உமிழ் வேதி மாற்றங்கள்:
இயற்பியல் மாற்றம் போலவே, வேதியியல் மாற்றமும் வெப்ப ஏற்பு மாற்றமாகவோ அல்லது வெப்ப உமிழ் மாற்றமாகவோ இருக்கலாம்.
இந்த செயல்பாட்டில், அம்மாணவர் சோப்புத் தூளுடன் நீரினைச் சேர்க்கும் பொழுது வெப்பமாக இருந்ததாகவும் குளுக்கோசுடன் நீர் சேர்த்த போது குளிர்ச்சியாக இருந்ததாக சொன்னார்.
மெக்னீசியம் நாடா எரியும்பொழுது வெப்பமும் ஒளியும் வெளியேறியதைப் பார்த்த நினைவிருக்கும். அதேபோல், மரம் எரியும்பொழுது வெப்பமும், ஒளியும் வெளியேறுகிறது. இம்மாதிரி வெப்பத்தை வெளியிடும் மாற்றங்களுக்கு வெப்ப உமிழ் மாற்றங்கள் என்றழைக்கப்படும்.
சில மாற்றங்களின் பொழுது வெப்பம் உறிஞ்சப்படுகிறது. எடுத்துக்காட்டாக, நீர் வெப்பத்தை உறிஞ்சி நீராவியாகிறது அதேபோல் பனிக்கட்டி வெப்பத்தை ஏற்று, உருகி நீராகிறது. இம்மாதிரி வெப்பத்தை உறிஞ்சும் மாற்றங்கள் வெப்ப ஏற்பு மாற்றங்கள் என்றழைக்கப்படும்.
கால – ஒழுங்கு மற்றும் கால – ஒழுங்கற்ற மாற்றம்:
மாற்றம் நிகழும் கால இடைவெளியின் அடிப்படையில், மாற்றங்களை கால ஒழுங்கு மாற்றம் அல்லது கால – ஒழுங்கற்ற மாற்றம் என்று வகைப்படுத்தலாம்.
கால ஒழுங்கு மாற்றங்கள்:
குறிப்பிட்ட கால இடைவெளியில் மாற்றங்களானது மீண்டும் நிகழ்ந்தால், அது கால ஒழுங்கு மாற்றங்கள் எனப்படும்.

பூமியின் சுழற்சி மற்றும் சுற்றுதல், இதயத்துடிப்பு, மணிக்கொரு முறை கடிகாரம் அடிக்கும் நிகழ்வு, கடிகாரத்தின் நொடி – முள்/நிமிட – முள்/மணி – முள்ளின் ஓட்டம் ஆகிய சில கால – ஒழுங்கு மாற்றங்களாகும்.
ஓவ்வொரு வருடமும் பருவங்கள் மாறுவது. மழைக்காலம் முதல் குளிர்காலம் வருவது மற்றும் குளிர்காலத்திலிருந்து கோடைக்காலம் வருவது போன்றவை. நாம் ஒவ்வொரு வருடமும் அனுபவிக்கும் மாற்றமாகும்.
குளிர்காலத்திலிருந்து நாம் கோடைக்காலம் வந்தவுடன், நாம் உடுத்தும் உடையின் தன்மையும் மாறுகிறது. குளிர்காலத்தில் கம்பளியிலான ஆடைகளையும், கோடைக்காலத்தில் பருத்தியிலான ஆடைகளையும் அணிகிறோம். ஏனெனில் குளிர்காலம் குளிர்ச்சியாகவும், கோடைக்காலம் வெப்பமாகவும் இருக்கும். குளிர்காலத்தில் இரவின் நீளம் கோடைக்காலத்தைவிட இருக்கும். கோடைக்காலத்தில் குளிர் பானங்களையும், குளிர்காலத்தில் சூடான தேநீர், காபி அல்லது பாலினை பருக விரும்புகிறோம். இம்மாற்றங்கள் பருவங்கள் மாறுவதால் ஏற்படும் சீதோஷணத்தைப் பொருத்தது.
பருவங்கள் மாறுவதும் அதைச் சார்ந்து வானிலை மாறுவதும் நிலையான அச்சில் சுழலும் பூமியின் சுழற்சியால் நிகழ்கிறது. இயற்கையில் பருவகால மாற்றங்கள் ஏற்படும் நிகழ்வு கால – ஒழுங்கு மாற்றமாகும்.
கால – ஒழுங்கற்ற மாற்றங்கள்:
ஒரு குறிப்பிட்ட கால இடைவெளியில் மீண்டும் நிகழாத மாற்றங்களும் சீரற்ற கால இடைவெளியில் நிகழும் மாற்றங்களும் கால – ஒழுங்கற்ற மாற்றங்களாகும். எரிமலை வெடித்தல், நிலநடுக்கம் ஏற்படுதல், இடியுடன் கூடிய மழைபொழிவின் பொழுது தோன்றும் மின்னல் கிரிக்கெட்டில் இரு புறமும் உள்ள ஸ்டம்புகளின் இடைப்பட்ட தொலைவில் ஓடும் ஆட்டக்காரரின் ஓட்டம், நடனம் ஆடுபவருடைய கால்களின் இயக்கம் ஆகிய சில நிகழ்வுகள் கால ஒழுங்கற்ற மாற்றங்களாகும்.

நினைவில் கொள்க:
- வெப்பப்படுத்தும் பொழுது பருப்பொருள்களில் அமைந்துள்ள துகள்களின் அமைப்பு பாதிப்படைகிறது. இந்த பாதிப்பை விரிவடைதலாகவோ, சுருக்கமடைதலாகவோ பார்க்கிறோம்.
- ஒரு திரவத்தினை வெப்பப்டுத்தி வாயு நிலைக்கு மாற்றும் முறைக்கு ஆவியாதல் என்று பெயர்.
- ஒரு திண்மத்தினை வெப்பப்படுத்தி, திரவநிலைக்கு மாற்றும் முறைக்கு உருகுதல் அல்லது கசிதல் என்று பெயர்.
- வாயு நிலையில் உள்ள நீர், நீர்ம நிலைக்கு மாறும் நிகழ்வுக்கு ஆவி சுருங்குதல் என்று பெயர்.
- திரவ நிலை பொருள் திண்ம நிலைக்கு மாறும் நிகழ்விற்கு உறைதல் என்று பெயர்.
- ஒரு பொருளின் வேதி இயைபில் மாற்றம் ஏதும் நிகழாமல் அதனுடைய இயற்பியல் பண்புகளில் மட்டும் ஏற்படும் மாற்றங்கள் இயற்பியல் மாற்றங்களாகும்.
- திண்மப் பொருள்கள் பெரும்பாலும் படிகமாக்குதல் முறையில் தூய்மை செய்யப்படுகிறது.
- திண்மம் – திரவக் கலவையில் கரைந்த நிலையில் உள்ள திண்மங்களை பிரித்தெடுக்க ஆவியாதல் என்ற நுட்பம் நிகழ்த்தப்படுகிறது.
- கற்பூரம், நாப்தலீன் போன்ற சில திண்மப் பொருள்களை வெப்பப்படுத்தும்பொழுது, திரவ நிலையை அடையாமல் நேரிடையாக வாயு நிலைக்குச் செல்வது பதங்கமாதல் என்று பெயர்.
- ஒரு பொருளின் வேதி இயைபில் மாற்றம் ஏற்பட்டு, புதிய பொருளாக உருமாறுவதோ அல்லது வேறு ஒரு புதிய பொருளாக உருவாவதோ வேதியியல் மாற்றங்களாகும்.
- ஒரு மாற்றமானது குறிப்பிட்ட கால இடைவெளியில் மீண்டும் நிகழ்ந்தால் அது கால ஒழுங்கு மாற்றமாகும்.
- குறிப்பிட்ட கால இடைவெளியில் மீண்டும் நிகழாமல் ஒழுங்கற்ற கால இடைவெளியில் நிகழும் மாற்றங்கள் கால – ஒழுங்கற்ற மாற்றங்களாகும்.
- செயல் நிகழும் பொழுது வெப்பத்தை ஏற்கும் மாற்றம் வெப்பம் – கொள் மாற்றமாகும்.
- செயல் நிகழும் பொழுது வெப்பத்தை உமிழும் மாற்றம் வெப்ப உமிழ் மாற்றமாகும்.
உங்களுக்கு தெரியுமா?
டெல்லியில் உள்ள இரும்புத்தூண் ஆச்சரியத்தக்க வகையில் துருப்பிடிக்கவில்லை! டெல்லியில் உள்ள குதூப் வளாகத்தில் 1600 ஆண்டுகள் பழமை வாய்ந்த ஒரு இரும்புத்தூண் உள்ளது. இவ்வளவு நூற்றாண்டுகள் கடந்தும், எந்தக் கூரையும் இன்றி புறவெளியில் உள்ள அந்த இரும்புத்தூண் துருப்பிடிக்கவில்லை. இதிலிருந்து 16ஆம் நூற்றாண்டிலேயே துருப்பிடித்தலை தவிர்க்கும் உலோகத் தொழில் நுட்பத்தில் இந்திய அறிவியலாளர்கள் சிறந்து விளங்கியது புலனாகிறது.
இரும்பின் மீது குரோமியம் அல்லது துத்தநாகம் போன்ற உலோகங்களை ஒரு படலமாகப் பூசுவதும் துருப்பிடித்தலைத் தடுக்கும் ஒரு மாற்று முறையாகும். இம்முறைக்கு நாக முலாம் பூசுதல் என்று பெயர். இம்முறையைப் பற்றி விரிவாக உயர்வகுப்புகளில் கற்க இருக்கிறீர்கள்.
லூயிஸ் பாஸ்டியர் (1822-1895) என்ற பிரெஞ்சு வேதியாலர் ஒரு நுண்ணுயிரியலாளரும் ஆவார். இவரே முதன்முதலில் நொதித்தல் என்ற நிகழ்வினை விவரித்தவர் ஆவார். காற்று அற்ற சூழலில், ஈஸ்ட் என்ற நுண்ணுயிரியின் முன்னிலையில் நிகழும் செயல் நொதித்தல் என்று கூறினார். இவரே ரேபிஸ் என்ற வெறிநாய்கடிக்கும் மருத்துவம் கண்டறிந்தவர்.
எந்த ஒரு பொருள் ஒரு வேதிவினையில் எந்த மாற்றத்திற்கும் உட்படாமல், வேதி மாற்றத்தின் வேகத்தினை மட்டும் துரிதப்படுத்துமோ அப்பொருளுக்கு வினையூக்கி என்று பெயர். எடுத்துக்காட்டாக சர்க்கரையின் நொதித்தலில் ஈஸ்ட்டில் உள்ள நொதிகள் வினையூக்கியாக செயல்படுகிறது.