தனிமங்களின் ஆவர்த்தன வகைப்பாடு Notes 10th Science Lesson 8 Notes in Tamil
தனிமங்களின் ஆவர்த்தன வகைப்பாடு Notes 10th Science Lesson 8 Notes in Tamil
அறிமுகம்:
விஞ்ஞானத்தில், வேதியியல் துறையில் 18ஆம் மற்றும் 19ஆம் நூற்றாண்டுகளில், துரித மாற்றங்கள் நிகழ்ந்தன. கி.பி. (பொ.ஆ) 1860ல் விஞ்ஞானிகளால் 60 தனிமங்களும் அவற்றின் நிறைகளும் கண்டுபிடிக்கப்பட்டிருந்தன. அவற்றுள் சில, பண்புகளில் ஒத்திருந்ததால், ஒரே தொகுதிகளில் வரிசைப்படுத்தப்பட்டன. இக்காலக்கட்டத்தில் வெவ்வேறு புதிய தனிமங்கள் வெவ்வேறு பண்புகளோடு கண்டு பிடிக்கப்பட்டன. ஒவ்வொரு தனிமத்தின் பண்புகளை தனித்தனியே அறிவதற்கு பதிலாக, அவற்றைத் தொகுதிகளாவும், தொடர்களாகவும் ஒருங்கிணைத்து, பின் பண்புகளை ஒப்பிட்டுப் பார்த்தல் எளிமையாக இருக்கும் என கருதப்பட்டது. காய்களையும், கனிகளையும் அவற்றின் பண்புகள் பொறுத்து வகைப்படுத்துவது போல தனிமங்களை ஆவர்த்தனப் பண்புகள் மூலம் வரிசைப்படுத்தலாம் என கருதினர். எனவே அறிஞர்கள் தக்க வழியில், தனிமங்களை வரிசைப்படுத்த பல முயற்சிகளை மேற்கொண்டனர். கடந்த ஒன்பதாம் வகுப்புப் பாடத்தில் தனிமங்களை வரிசைப்படுத்த நடந்த முந்தைய முயற்சிகளைப் பற்றி அறிந்தீர்கள். ஒன்பதாம் வகுப்பில் தனிமங்களை வகைப்படுத்துதல் பாடத்தில் பெற்ற அறிவின் தொடர்ச்சியாக, நாம் உயர் சிந்தனைகளோடு முன் தொடர்ந்து, தனிமங்களின் பண்புகளைப் பற்றிய அறிவை வளர்த்துக் கொள்வோம்.
நவீன ஆவர்த்தன விதி:
மென்டலீபின் ஆவர்த்தன அட்டவணையில் தீர்க்க முடியாத சில முரண்பாடுகள் இருந்தன. உதாரணமாக அணுநிறை (39.95 amu) கொண்ட ஆர்கான் தனிமம், முன்னாலும், அணு நிறை (39.10 amu) கொண்ட பொட்டாசியம் தனிமம் பின்னாலும் வரிசைப்படுத்தப்பட்டன. அணுநிறையை மையமாகக் கொண்டு அடுக்குவோமாயின், பொட்டாசியத்தின் இடத்தை, ஆர்கான் பெற்றிருக்கும். லித்தியம் சோடியம் உள்ள தொகுதியில் ஆர்கானை எந்த ஒரு வேதியலாளரும் வைக்க மாட்டார்கள். இவை, அணுநிறை என்ற அடிப்படையை விட வேறு ஒரு அடிப்படைப் பண்பிற்கு வழிவகுத்தன. மெண்டலீப் மற்றும் அவரோடு இருந்தவர்களுக்கு அணுவில் உள்ள புரோட்டான்களின் எண்ணிக்கை அடிப்படை பண்பாக இருக்கிறது என்பது அறியக்கூடாததாய் இருந்தது.
1912ஆம் ஆண்டு ஹென்றி மோஸ்லே என்ற பிரிட்டன் விஞ்ஞானி ஆவர்த்தன வரிசைப்படுத்தலுக்கு, அணு எண் என்பது சிறந்த அடிப்படை என்ற உண்மையைக் கண்டறிந்தார். அணு எண் என்பது ஒரு அணுவின் உள்ள புரோட்டானின் எண்ணிக்கையையோ, அல்லது எலக்ட்ரானின் எண்ணிக்கையையோ குறிக்கும். ஆகவே ஆவர்த்தன விதியைக் கீழ்க்கண்டவாறு மேம்படுத்தி அறியலாம்.
“தனிமங்களின் இயற்பியல் மற்றும் வேதியியல் பண்புகள், அவற்றின் அணு எண்களைச் சார்ந்து அமையும்.”
நவீன ஆவர்த்தன அட்டவணை:
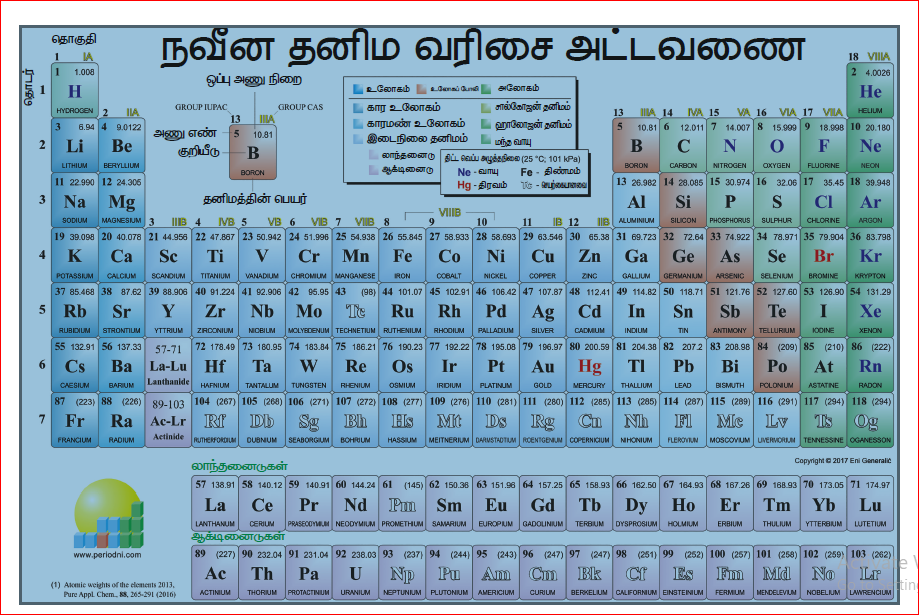
நவீன ஆவர்த்தன விதியின் படி, தனிமங்கள், அணு எண் அதிகரிப்பிற்கு ஏற்றாற்போல் நவீன அட்டவணையில் வரிசைப்படுத்தப்பட்டுள்ளன. வேதியியல் தனிமங்கள், தங்கள் பண்புகளை முறையே உணர்த்தும் வகையில், தொடர்களாகவும், தொகுதிகளாகவும், நவீன ஆவர்த்தன அட்டவணையில் வரிசைப்படுத்தப்பட்டுள்ளன. படமானது 118 தனிமங்கள் கொண்ட நவீன ஆவர்த்தன அட்டவணையைக் காட்டுகின்றது.
கடந்த ஒன்பதாம் வகுப்பில் கற்ற ஆவர்த்தன அட்டவணையின் சிறப்பம்சங்களின் தொடர்ச்சியாக, தொகுதி மற்றும் தொடர்களின் சிறப்பம்சங்களை அறிய விழைவோம்.
தொடர்களின் சிறப்பம்சங்கள்:
- தனிமங்களின் கிடைமட்ட வரிசைகள் தொடர்களாகும். ஆவர்த்தன அட்டவணையில் மொத்தம் 7 தொடர்கள் உள்ளன.
- முதலாம் தொடர் (அணு எண் 1 மற்றும் 2) இத்தொடர் மிகச்சிறிய தொடராகும். இதில் ஹைட்ரஜன் மற்றும் ஹீலியம் எனும் 2 தனிமங்களே உள்ளன.
- இரண்டாம் தொடர் (அணு எண் 3 லிருந்து 10 வரை) இது சிறிய தொடராகும். இதில் “Li” யிலிருந்து “Ne” வரை 8 தனிமங்கள் உள்ளன.
- மூன்றாம் தொடர் இதுவும் ஒரு சிறிய தொடராகும். (அணு எண் 11 லிருந்து 18 வரை) இதில் “Na” யிலிருந்து “Ar” வரை 8 தனிமங்கள் உள்ளன.
- நான்காம் தொடர் (அணு எண் 19 லிருந்து 36 வரை) இது ஒரு நீண்ட தொடராகும். இதில் “K”யிலிருந்து, “Kr”வரை, 18 தனிமங்கள் உள்ளன. இவற்றில் 8 பிரதிநிதித்துவ தனிமங்களும், 10 இடைநிலைத் தனிமங்களும் உள்ளன.
- ஐந்தாம் தொடர் (அணு எண் 37 லிருந்து, 54 வரை) இதுவும் ஒரு நீண்ட தொடராகும். இதில் Rb யிலிருந்து Xe வரை 18 தனிமங்கள் உள்ளன. இவற்றில் 8 பிரதிநிதித்துவ தனிமங்களும், 10 இடைநிலைத் தனிமங்களும் உள்ளன.
- ஆறாம் தொடர் (அணு எண் 55 லிருந்து 86 வரை) இது மிக நீண்ட தொடராகும். இதில் “Cs” லிருந்து, “Rn” வரை 32 தனிமங்கள் உள்ளன. இவற்றுள் 8 பிரதிநிதித்துவ தனிமங்கள், 10 இடைநிலைத் தனிமங்கள் மற்றும் 14 உள் இடைநிலைத் தனிமங்கள் (லாந்தனைடுகள்) என ஆகும்.
- ஏழாம் தொடர் (அணு எண் 87லிருந்து, 118 வரை) ஆறாம் தொடரைப் போல, இதுவும் 32 தனிமங்கள் கொண்டது. சமீபத்தில், நான்கு தனிமங்கள் அட்டவணையில் IUPACஆல் உட்படுத்தப்பட்டன.
தொகுதிகளின் சிறப்பம்சங்கள்:
- ஆவர்த்தன அட்டவணையில் மேலிருந்து கீழாக வரிசைப்படுத்தப்பட்ட தனிமங்கள், தொகுதிகள் எனப்படும். அட்டவணையில் மொத்தம் 18 தொகுதிகள் உள்ளன.
- தனிமங்களின் பொதுவான சிறப்பில்புகளை வைத்து வெவ்வேறு குடும்பங்களாகத் தொகுக்கப்பட்டுள்ளன.
- தொகுதி 3ன் அங்கமாகத் திகழும், லாந்தனைடு மற்றும் ஆக்டிணைடுகள் உள் இடைநிலைத் தனிமங்கள் என அழைக்கப்படும்.
- 18வது தொகுதியைத் தவிர, மற்ற தொகுதிகளில் உள்ள தனிமங்களின் வெளிக்கூட்டில், ஒத்த எண்ணிக்கை உள்ள எலக்ட்ரான்களும், ஒத்த இணைதிறனும் பெற்றிருக்கும். எடுத்துக்காட்டாக, தொகுதி 1 ல் உள்ள
| தொகுதி எண் | குடும்பம் |
| 1 | கார உலோகங்கங்கள் |
| 2 | காரமண் உலோகங்கள் |
| 3-12 | இடைநிலை உலோகங்கள் |
| 13 | போரான் குடும்பம் |
| 14 | கார்பன் குடும்பம் |
| 15 | நைட்ரஜன் குடும்பம் |
| 16 | ஆக்ஸிஜன் குடும்பம் (அ) சால்கோஜன் குடும்பம் |
| 17 | ஹேலஜன்கள் |
| 18 | மந்த வாயுக்கள் |
தனிமங்கள் வெளி ஆற்றல் மட்டத்தில் ஒரு எலக்ட்ரான் மட்டும் “1S” பெற்றிருப்பதால், கார உலோகத் தனிமங்களின் இணைதிறன் 1 ஆகும்.
- ஒத்த தொகுதியில் உள்ள தனிமங்கள் ஒத்த எலக்ட்ரான் அமைப்புகளைப் பெற்று, ஒத்த வேதிப்பண்புகளோடு திகழும்.
- இயல் பண்புகளான, உருகுநிலை, கொதிநிலை மற்றும் அடர்த்தி ஆகியன சீராக மாறுபடும்.
- 18வது தொகுதித் தனிமங்கள், நிலையான எலக்ட்ரான் அமைப்பை வெளிக்கூட்டில் பெற்றிருப்பதால், வினையுறா தன்மையைப் பெற்றிருக்கும்.
ஆவர்த்தன பண்புகளில் ஏற்படும் நிகழ்வுகள்:
தனிமங்களின் எலக்ட்ரான் அமைப்பு, சீராக நிகழும் இயல் மற்றும் வேதியியல் பண்புகளை விளக்க உதவுகின்றன. தனிம வரிசை அட்டவணையில் உள்ள தனிமங்களின் பண்புகள், குறிப்பிட்ட சீரான இடைவெளிக்குப் பிறகு மீண்டும் ஒரே மாதிரியிருக்கும் நிகழ்வு ஆவர்த்தன பண்பு எனப்படும்.
பண்புகளான, அணு ஆரம், அயனி ஆரம், அயனியாக்கும் ஆற்றல், எலக்ட்ரான், கவர்தன்மை, எலக்ட்ரான் நாட்டம் ஆகியன ஆவர்த்தனப் பண்பை காட்டுகின்றன. நவீன அட்டவணையானது தனிமங்களின் பொதுப்பண்புகளையும், தொகுதி மற்றும் தொடர்களில் ஏற்படும் தனிமங்களின் சீரான மாற்றங்களையும் அறிமுகமாகாத தனிமங்களுக்கும் மிகத் தெளிவாகத் தருகின்றது. இப்பகுதியில் பின்வரும் ஆவர்த்தன பண்புகளைப் பற்றி அறியலாம்.
அணு ஆரம்:
ஒரு அணுவின் ஆரம் என்பது அதன் அணுக்கருவின் மையத்திற்கும், இணைதிற எலக்ட்ரான் உள்ள வெளிக்கூட்டிற்கும் இடையேயான தூரம் என வரையறுக்கப்படும். ஒரு தனித்த அணுவின் ஆரத்தை, நேரடியாக அளவிட முடியாது. மந்த வாயுக்கள் தவிர, வழக்கமாக அணு ஆரம் என்பது தொடர்புடைய அணுக்களுக்கிடையே உள்ள பிணைப்பின் தன்மையை பொறுத்து, சகப்பிணைப்பு ஆரம் அல்லது உலோக ஆரம் என்றழைக்கப்படும். அருகருகே உள்ள இரண்டு உலோக அணுக்களின் உட்கருக்களுக்கு இடையே உள்ள தூரத்தின் பாதியே உலோக ஆரம் எனப்படும்.
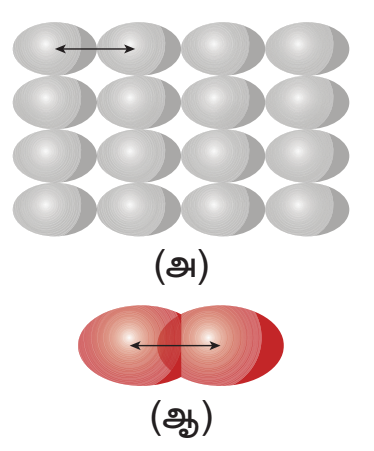
அ. உலோக ஆரம்
ஆ.சகப்பிணைப்பு ஆரம்
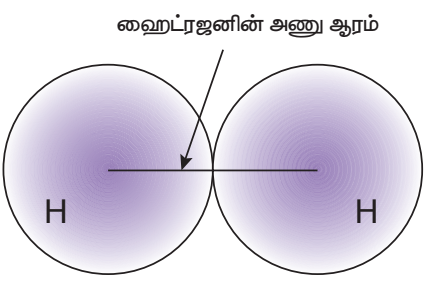
ஹைட்ரஜனின் அணு ஆரம்
அ. உலோகமற்ற தனிமங்களில், உள்ள அணு ஆரம் சகப்பிணைப்பு ஆரம் என்றழைக்கப்படும். ஒற்றை சகப்பிணைப்பால் பிணைக்கப்பட்டுள்ள இரண்டு ஒத்த அணுக்களின் அணுக்கருக்களுக்கு இடையே ஆன தொலைவின் பாதியளவு சகப்பிணைப்பு ஆரம் எனப்படும். எடுத்துக்காட்டாக, H2 மூலக்கூறில், இரண்டு ஹைட்ரஜன் அணுக்கருகளுக்கு இடையில் உள்ள தூரம் 0.74A0. இதன் சகப்பிணைப்பு ஆரமானது. 0.74/2 = 0.37A0 என்று கணக்கிடலாம்.
தனிம வரிசை அட்டவணையில் உள்ள தனிமங்களின் அணு ஆரங்களைப் பார்க்கும் போது, இருவேறு நிகழ்வுகள் தெளிவாகும். தொடரில், இடது புறத்திலிருந்து வலதுபுறமாக செல்கையில், தனிமங்களின் அணு ஆரங்கள் குறையும். ஆனால் தொகுதியில் மேலிருந்து கீழாக இறங்கும்போது அணு ஆரங்கள் அதிகரிக்கும். இதன் காரணத்தை கீழ்க்கண்டவாறு அறியலாம். தொகுதியில் மேலிருந்து கீழாக இறங்கும் போது, வெளிக்கூடு எண் அதிகரிக்கும் இதனால், வெளிக்கூட்டிற்கும் ஆற்றல் மட்டத்திற்கும் அணுக்கருவிற்கும் இடைப்பட்ட தூரம் அதிகரித்து கவர்ச்சி விசை குறைந்து, உருவளவு பெரிதாகக் காணப்படும்.
மாறாக தொடரில் இடது புறத்திலிருந்து வலதுபுறமாக செல்கையில், ஆற்றல் மட்டம் மாறுவதில்லை. ஆனால் புரோட்டானின் எண்ணிக்கை அதிகரித்து செல்லும். அதிகரிக்கும் நேர்மின் சுமைக்கு ஏற்ப எலக்ட்ரான்கள் மீதுள்ள கவர்ச்சி விசை அதிகரிப்பதால் அணுவின் உருவ அளவு குறைகிறது. அணு ஆரமானது லித்தியத்திலிருந்து போரானுக்கு செல்லும் போது எவ்வாறு குறைகிறது என்பதை படம் காட்டுகின்றது.
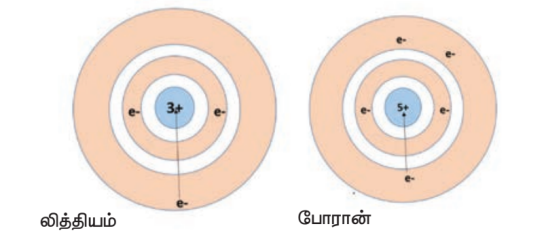
அணு ஆரம் மாறுபாடு
அயனி ஆரம்:
ஒரு அயனியில் கருமையத்திற்கும், அவ்வயனியின் எலக்ட்ரான் திரள் முகில் மீது அதன் கருவால் கவர்ச்சி விசை செலுத்த இயலும் தூரத்திற்கும் இடையேயான தொலைவு அயனி ஆரம் என வரையறுக்கப்படும். ஒரு அணுவானது எலக்ட்ரான்களை இழந்தோ, ஏற்றோ அயனியாக மாறும். எலக்ட்ரான் இழக்கும் அணு, நேர்மின் சுமை பெற்று, நேர்மின் அயனி என்றழைக்கப்படும் எலக்ட்ரானை ஏற்கும் “அணு, எதிர் மின்சுமை பெற்று, எதிர்மின் அயனி என்றழைக்கப்படும். கரைசல்களின் இயல்புகளையும், அயனித்திண்மங்களின் வடிவமைப்புகளையும், தீர்மானிக்க, அயனிகளின் உருவளவு முக்கியமாகும். நேர்மின் அயனியானது அதன் தொடர்புடைய அணுவைவிட உருவளவில் சிறிதாகவும், எதிர்மின் அயனியானது அதன் தொடர்புடைய அணுவைவிட உருவளவில் பெரிதாகவும் காணப்படும்.
குறிப்பு:
- நேர்மின் சுமை அதிகரிக்கும் போது நேர்மின் அயனியின் உருவளவு குறையும்.
- எதிர் மின்சுமை அதிகரிக்கும் போது எதிர்மின் அயனியின் உருவளவு அதிகரிக்கும்.

பிகா மீட்டரில் ஆரம்
நேர் மற்றும் எதிர்மின் அயனிகளின் ஓப்பீட்டு ஆரங்கள்:
உதாரணமாக லித்தியம் மற்றும் சோடியம் தங்களது வெளி ஆற்றல் மட்டத்தில் உள்ள ஓர் எலக்ட்ரானை இழந்து நேர்மின் அயனிகளாகின்றன. இவ்வயனிகள், தம் தொடர்புடைய அணுக்களைவிட உருவில் சிறிதாக இருக்கக் காரணம், உட்கருவிற்கும், மீதமுள்ள உள் ஆற்றல் மட்ட எலக்ட்ரான்களுக்கும் இடையே உள்ள அதிக கவர்ச்சி விசையே காரணம் ஆகும். ப்ளுரின் மற்றும் குளோரின் தங்களது வெளிக்கூட்டில் ஒரு எலக்ட்ரானை ஏற்று எதிர்மின் சுமையுடைய அயனிகளாகின்றன. உட்கருவானது எதிர்மின் சுமையுடைய அயனிகளில் உள்ள வெளிக்கூட்டு எலக்ட்ரான்களில் காட்டும் ஈர்ப்பு விசையானது அதே தனிமத்தின் நடுநிலை அணுவில் காட்டுவதை விட குறைவு. ஆகவே அணு ஆரத்தில் கண்டது போல, அயனி ஆரங்களும் தொடரில் இடப்புறத்திலிருந்து வலப்புறமாக குறைந்தும், தொகுதியில், மேலிருந்து கீழாக அதிகரித்தும் காணப்படும்.
அயனியாக்கும் ஆற்றல்:
அடி ஆற்றல் நிலையில் (Ground State) உள்ள நடுநிலைத் தன்மை உடைய தனித்த வாயு நிலை அணு ஒன்றின் இணைதிறன் கூட்டிலிருந்து இலகுவாகப் பிணைக்கப்பட்டுள்ள ஒரு எலக்ட்ரானை நீக்கி நேர்மின் அயனியாக மாற்றுவதற்கு தேவைப்படும் குறைந்த பட்ச ஆற்றல், அயனியாக்கும் ஆற்றல் எனப்படும். இதை அயனியாக்கும் என்தால்பி என்றும் அழைக்கலாம். இதன் அலகு KJ/mol. அயனியாக்கும் ஆற்றல் அதிகரிக்கும்போது, எலக்ட்ரானை நீக்குவது கடினமாகின்றது.
தொடரில் அணு ஆரம் இடது புறத்திலிருந்து வலது புறமாக செல்கையில் குறைவதால், எலக்ட்ரானை நீக்க, அதிக ஆற்றல் தேவைப்படும். ஆகவே, தொடரில், இடது புறத்திலிருந்து வலதுபுறம் செல்கையில், அயனி ஆக்கும் ஆற்றல் அதிகரிக்கின்றது. ஆனால் தொகுதியில் மேலிருந்து கீழாக இறங்குகையில், அணுவின் உருவளவு அதிகரிப்பதாலும், இணைதிற எலக்ட்ரான்கள் இலகுவாக பிணைக்கப்பட்டிருப்பதாலும், அயனியாக்கும் ஆற்றல் மிகச் சிறிதளவே தேவைப்படும். ஆகவே, தொகுதியில் மேலிருந்து கீழிறங்குகையில் அயனியாக்கும் ஆற்றல் குறையும் தன்மை பெற்றிருக்கும்.
எலக்ட்ரான் நாட்டம்:
ஒரு தனித்த நடுநிலை உடைய வாயுநிலை அணு ஒன்றின் இணைதிறன் கூட்டில், ஒரு எலக்ட்ரானை சேர்த்து, அதன் எதிர் மின் சுமையுடைய அயனியை உருவாக்கும் போது வெளிப்படும் ஆற்றல் எலக்ட்ரான் நாட்டம் எனப்படும். அயனியாக்கும் ஆற்றலைப் போல, எலக்ட்ரான் நாட்டமும் தொடரில் இடப்புறத்திலிருந்து, வலப்புறமாக அதிகரித்தும், தொகுதியில் மேலிருந்து கீழாக குறைந்தும் காணப்படும்.
இதன் அலகு KJ/mol ஆகும்.
A(g) + e– ???? A–(g) + ஆற்றல்
Cl(g) + e– ???? Cl–(g) + ஆற்றல்
எலக்ட்ரான் கவர்தன்மை
சகப்பிணைப்பால் பிணைக்கப்பட்டுள்ள மூலக்கூறில் உள்ள ஒரு அணுவானது, சகப்பிணைப்பில் பங்கிடப்பட்டுள்ள எலக்ட்ரான் இணையினை தன்னை நோக்கி கவரும் பண்பு, எலக்ட்ரான் கவர்திறன் எனப்படும். உதாரணமாக HCI மூலக்கூறை எடுத்துக் கொள்வோம். ஹைட்ரஜன் மற்றும் குளோரின் அணுக்கள் ஒரு எலக்ட்ரானை பங்கிட்டு சகப்பிணைப்பினை உருவாக்கும். குளோரின் அணுவிற்கு எலக்ட்ரான் கவர்தன்மை அதிகம். அதனால், பங்கீட்டு எலக்ட்ரான்களை ஹைட்ரஜன் விட, குளோரின் அணு தன்னை நோக்கி இழுத்துக் கொள்ளும். பிணைப்பு உடையும்போது பிணை எலக்ட்ரான், குளோரினுடன் சென்று H+ மற்றும் CI–அயனிகள் உருவாகும். இதை கீழ்க்காணும் படங்களின் மூலம் அறியலாம்.

ஹைட்ரஜனுக்கும், குளோரினுக்கும் உள்ள ஒப்பீட்டு எலக்ட்ரான் கவர்தன்மை
எலக்ட்ரான் கவர்தன்மையானது கீழ்க்காணும் சோதனை முடிவுகளான, பிணைப்பு ஆற்றல், அயனியாக்கும் ஆற்றல், எலக்ட்ரான் நாட்டம் ஆகியவற்றைச் சார்ந்து அமையும்.
எலக்ட்ரான் கவர்தன்மையை கணக்கிடுவதில், பாலிங் அளவீடு பெரும் பங்களிக்கின்றது. இதன் மூலம், ஒர மூலக்கூறின் அணுக்களுக்கு இடையில் உள்ள பிணைப்பின் தன்மையை (அயனிப்பிணைப்பு அல்லது சகப்பிணைப்பு) அறியலாம்.
சில தனிமங்களின் எலக்ட்ரான் கவர்தன்மையைக் கீழே காண்க.
F = 4.0, Cl = 3.0, Br = 2.8, I = 2.5, H = 2.1, Na = 1
இரு அணுக்களுக்கு இடையே உள்ள எலக்ட்ரான் கவர்தன்மை வித்தியாசம் 1.7 என இருந்தால், அப்பிணைப்பு 50% அயனித்தன்மையும், 50% சகப்பிணைப்புத் தன்மையையும் பெற்றிருக்கும்.
அவ்வித்தியாசம் 1.7 ஐ விட குறைவாயின் அப்பிணைப்பு அதிக சகப்பிணைப்பு தன்மையுடையது.
வித்தியாசமானது 1.7 ஐ விட அதிகமெனில் அப்பிணைப்பு அதிக அயனிப்பிணைப்பு தன்மையுடையது.
தொடரில், இடப்பக்கத்திலிருந்து வலப்பக்கமாக செல்லும் போது எலக்ட்ரான் கவர்தன்மை அதிகரிக்கும். ஏனெனில் அணுக்கரு மின்சுமை அதிகரிக்கும்போது, எலக்ட்ரான் கவர்ச்சி விசை அதிகமாகும். தொகுதியில் மேலிருந்து கீழாக இறங்குகையில் எலக்ட்ரான் கவர்தன்மை குறைகிறது. ஏனெனில், ஆற்றல் மட்டத்தின் எண்ணிக்கை அதிகமாகிறது.
| ஆவர்த்தனப் பண்பு | தொடரில் மாற்றம் | தொகுதியில் மாற்றம் |
| அணு ஆரம் | குறைகிறது | அதிகரிக்கிறது |
| அயனி ஆரம் | குறைகிறது | அதிகரிக்கிறது |
| அயனயாக்கும் ஆற்றல் | அதிகரிக்கிறது | குறைகிறது |
| எலக்ட்ரான் நாட்டம் | அதிகரிக்கிறது | குறைகிறது |
| எலக்ட்ரான் கவர்தன்மை | அதிகரிக்கிறது | குறைகிறது |
உலோகவியல்:
மனித வாழ்வு வெவ்வேறு உலோகங்களுடன் தொடர்புடையது. அன்றாட வாழ்வியலில், உலோகங்களை நாம் பயன்படுத்துகிறோம். மனித உடலில் சோடியம், பொட்டாசியம், கால்சியம், இரும்பு முதலான உலோகங்கள் இன்றியமையா இடம் பெற்றுள்ளன. இவ்வுலோகங்களின் குறைபாடுகள் வளர்சிதை மாற்றங்களைப் பாதித்து, நோய்கள் உருவாகக் காரணமாகும். ஆகவே, உலோகங்கள், நம் வாழ்வில் முக்கிய பங்கு வகிக்கின்றன. இப்பகுதியில், உலோகவியல் மூலம் உலோகங்கள் எவ்வாறு பிரித்தெடுக்கப்படுகின்றன என்பதை விவரிக்கலாம்.
உலோகங்களை அவற்றின் தாதுக்களிலிருந்து பிரித்தெடுத்து, இயல் மற்றும் வேதியியல் பண்புகளுக்கு ஏற்றாற்போல் அவற்றை உலோகக் கலவைகளாக மாற்றி, வெவ்வேறு பயன்பாட்டுக்கு உட்படுத்தும் அறிவியலே உலோகவியல் எனப்படும். உலோகவியலின் செயல்பாடுகள் மூன்று படிகளைக் கொண்டது.
- தாதுக்களை அடர்ப்பித்தல் இம்முறையின் மூலம், தாதுக்களில் உள்ள மாசுக்கள் நீக்கப்படுகின்றன.
- உலோகத்தை உருவாக்கல் இம்முறையில், தாதுவில் இருந்து உலோகம் பிரித்தெடுக்கப்படுகிறது.
- உலோகத்தை தூய்மையாக்கல் இம்முறையில் உலோகமானது தூய்மை செய்யப்படுகிறது.
உலோகவியலில் உள்ள கலைச் சொற்கள்:
கனிமங்கள்: ஒரு கனிமம் என்பது தனி சேர்மமாகவோ அல்லது வெவ்வேறு சேர்மங்களைச் சேர்த்து அடக்கிய கூட்டுக் கலவையாகவோ புவியில் காணப்படும்.
தாது: எக்கனிமத்திலிருந்து, உலோகமானது எளிதில், சிக்கனமாக, பெரிய அளவில் பிரித்தெடுக்க முடிகிறதோ அதுவே தாது எனப்படும்.
உதாரணமாக களிமண்ணும், (Al2O2.2SiO2.2H2O) பாக்சைட்டும் (Al2O3.2H2O) அலுமினியத்தின் கனிமங்களாகும். ஆனால், பாக்சைட்டிலிருந்து அலுமினியம் இலாபகரமாக பிரித்தெடுக்கமுடிவதால், பாக்சைட்டானது அலுமினியத்தின் தாது என்றும், களிமண் அதன் கனிமம் என்றும் அழைக்கப்படும்.
சுரங்க உற்பத்தி: புவித் தோட்டிலிருந்து, தாதுக்களைப் பிரிக்கும் முறையே சுரங்க உற்பத்தி எனப்படும்.
தாதுக்கூளம் அல்லது காங்கு: உலோகத் தாதுப்பொருட்களோடு கலந்துள்ள மண் மற்றும் பாறைத் தூள் மாசுக்கள் காங்கு அல்லது தாதுக்கூளம் எனப்படும்.
இளக்கி: தாதுவுடன் உள்ள மாசுக்ளை (காங்கு) உருகிடும் சேர்மமாக மாற்றி, அதை நீக்கிட தாதுவுடன் சேர்க்கும் பொருளே இளக்கி எனப்படும். எ.கா: CaO(காரத்தன்மையது), SiO (அமிலத்தன்மையது).
கசடு: உலோகத்தைப் பிரித்தலில், இளக்கி தாதுக்கூளத்துடன் வினைபுரிந்து உருவாக்கும் விளைபொருளே கசடு எனப்படும்.
தாதுக்கூளம் + இளக்கி ????கசடு
உருக்கிப்பிரித்தல்: வறுத்த உலோக ஆக்சைடை, உலோகமாக உருகிய நிலையில், மாற்றும் ஒரு ஒடுக்கவினையே உருக்கிப்பிரித்தல் ஆகும். இம்முறையில் காங்கு எனப்படும் மாசுக்கள், சேர்க்கப்பட்ட இளக்கியால் கசடாக நீக்கப்படுகின்றன.
தாதுக்களை பிரித்தெடுக்கும் முறைகள் அல்லது அடர்ப்பிக்கும் முறைகள்:
தாதுக்களின் இயல்பைப்பொறுத்து, அவற்றிலிருந்து உலோகத்தைப் பிரித்தெடுக்கும் முறையாது நான்கு வகைப்படும். அட்டவணையில் உலோகங்களின் வெவ்வேறு தாதுக்கள் பட்டியலிடப்பட்டுள்ளது.
நன்கு தூளாக்கப்பட்ட தாதுக்களை அடர்ப்பிக்கும் முறைகள் கீழ்க்கண்டவாறு அமைகின்றன.
- புவியீர்ப்பு முறையில் பிரித்தல்:
தத்துவம்: தாதுக்களுக்கும், தாதுக் கூளங்களுக்கும், இடையில் உள்ள அடர்த்தி வேறுபாடு இம்முறையின் அடிப்படையாகும். ஆக்சைடு தாதுக்கள் இம்முறையினால் தூய்மையாக்கப்படுகின்றன. எ.கா: ஹேமடைட் Fe2O3 (இரும்பின் தாது).
குறிப்பு: தாதுவானது அதில் கலந்துள்ள மாசுக்களைவிட கனமானதாக (அடர்த்தி மிகுந்ததாக) இருக்கும்போது இப்பிரித்தெடுத்தல் முறை பயன்படுகிறது.
முறை: நன்கு தூளாக்கப்பட்ட தாது, அதிர்வடையும் சாய் தளத்தின் மேல் கொட்டப்படும். பிறகு நீர் அதன் மேல் பீய்ச்சிஅடிக்கப்படும். இதனால், அடர்த்தி மிகு தாது தூள்கள் கீழே தங்கி விட லேசான தாதுக்கூளங்கள், தண்ணீரால் கழுவி நீக்கப்படுகின்றன.
- காந்த முறை பிரிப்பு:
தத்துவம்: தாதுக்களின் காந்தத்தன்மை, பிரித்தலின் அடிப்படையாக அமைகிறது. தாதுவோ அல்லது தாதுக்கூளமோ காந்தத் தன்மை பெற்றிருப்பின், இம்முறை செயல்படுத்தப்படும். எ.கா:டின்ஸ்டோன் SnO2 வெள்ளீயத்தின் தாது.
முறை: நன்கு தூளாக்கப்பட்ட தாதுவானது இரண்டு உலோக உருளைகளுக்கு ஊடே செல்லும் இயங்கு பெல்டின் மூலம் கொட்டப்படுகின்றது. இவ்உருளைகளில் ஒன்று காந்தத் தன்மையுடன் இருப்பதால், காந்தத் துகள்கள், காந்த தன்மையுள்ள உருளையால் ஈர்க்கப்பட்டு காந்த தன்மையற்ற துகள்கள் தொலைவில் செறிந்து பிரிக்கப்படும்.
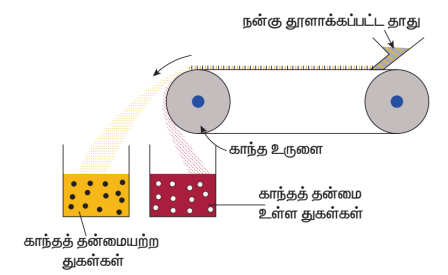
காந்தமுறையில் பிரித்தல்
- நுரை மிதப்புமுறை:
தத்துவம்: பைன் ஆயிலின் மூலம் தாதுக்களையும், நீரின் மூலம் தாதுக்கூளங்களையும் எந்த அளவிற்கு எளிதில் ஈரப்பதம் ஏற்ற முடியுமோ, அதுவே, இம்முறையின் தத்துவமாகும். லேசான தாதுக்களான, சல்பைடு தாதுக்கள், இம்முறையில் அடர்ப்பிக்கப்படுகின்றன. எ.கா: ஜிங்க் ப்ளன்ட் ZnS.
குறிப்பு: தாதுவானது அதில் கலந்துள்ள மாசுக்களைவிட இலேசானதாக (அடர்த்தி குறைவாக) இருக்கும்போது இப்பிரித்தெடுத்தல் முறை பயன்படுகிறது.

நுரைமிதப்பு முறை
முறை: நன்கு தூளாக்கப்பட்ட தாதுவானது, எண்ணெயும், நீரும் கொண்ட ஒரு பெரிய தொட்டியில் இடப்பட்டு, அவற்றின் மேல் நன்கு அழுத்தப்பட்ட காற்று செலுத்தப்படுகின்றது. தாதுவானது எண்ணெயின் மூலம் ஈரப்படுத்தப்பட்டு நுரைவடிவில், தாதுக்கூளத்திலிருந்து பிரிக்கப்படுகின்றது. தாதுவானது லேசாக உள்ளதால் அது நுரைவடிவில் வெளிப்பரப்பிற்கு வந்துவிடும், மாசுக்கள் அடியில் தங்கிவிடும். எ.கா: ஜிங்க் ப்ளன்ட் (ZnS).
- வேதிமுறை: மிக தூய நிலையில் உள்ள தாதுக்களை அடர்பிப்பதற்கு இம்முறை பயன்படுத்தப்படுகிறது.
தாதுவானது தகுந்த வேதிப்பொருளுடன் வினைபுரிய செய்து கரையச் செய்வதன் மூலம், கரையாத மாசுக்கள் வடிக்கட்டலின் மூலம் பிரித்தெடுக்கப்படுகின்றன. வடிநீர் தகுந்த வேதிப்பொருளுடன் சேர்க்கப்பட்டு, வினைபுரிந்து தாது வீழ்படிவாக மாறுகின்றது. எ.கா:பாக்சைட் Al2O3.2H2O (அலுமினியத்தின் முக்கிய தாது).
தமிழ்நாட்டில் கிடைக்கும் தாதுக்கள்:
சுண்ணாம்புக்கல்: கோவை, கடலூர், திண்டுக்கல்.
ஜிப்சம்: திருச்சி, கோவை மாவட்டங்கள்.
டைட்டேனிய கனிமங்கள்: கன்னியாகுமரி, நெல்லை மற்றும் தூத்துக்குடி.
குரோமைட்: கோவை, சேலம் மாவட்டங்கள்.
மேக்னடைட்: தர்மபுரி, ஈரோடு, சேலம், திருவண்ணாமலை.
டங்க்ஸ்டன்: மதுரை, திண்டுக்கல்.
உலோகத்தின் பண்புகள்:
இயற்பண்புகள்:
- இயல்புநிலை: எல்லா உலோகங்களும், அறை வெப்பநிலையில் திட நிலையில் உள்ளவை. (மெர்குரி மற்றும் காலியம் தவிர).
- பளபளப்புத் தன்மை: உலோகங்கள் அதிக பளபளப்பானவை.
- கடின தன்மை: அனேக உலோகங்கள், கடின தன்மையையும் வலிமையையும் பெற்றவை (சோடியம், பொட்டாசியம் தவிர. இவை கத்தியால் வெட்ட இயலும் மென்மை பெற்றவை).
- உருகுநிலை மற்றும் கொதிநிலை: வழக்கமாக, உலோகங்கள் அதி உருகுநிலை மற்றும் கொதிநிலையைப் பெற்றிருக்கும். அதிக வெப்பநிலையில், அவை ஆவியாகும். (காலியம், மெர்குரி, சோடியம், பொட்டாசியம் தவிர).
- அடர்த்தி: உலோகங்கள் அதிக அடர்த்தி பெற்றவை. (சோடியம் மற்றும் பொட்டாசியம் தவிர இவை தண்ணீர் விட அடர்த்தி குறைந்தவை).
- கம்பியாக நீளும் தன்மை: உலோகங்கள் கம்பியாக நீளும் தன்மையன. அவற்றை உடைக்காமல், கம்பியாக நீட்ட முடியும்.
- தகடாகும் தன்மை: உலோகங்கள் தகடாகும் தன்மை பெற்றவை. அதாவது, அவற்றை எந்த பிளவும்படாமல், அடித்தடித்து தகடாக மாற்ற முடியும்.
- வெப்பம் மற்றும் மின்கடத்தும் தன்மை: உலோகங்கள் வெப்பத்தையும், மின்சாரத்தையும்
தாதுக்களின் வகைகள்
| ஆக்சைடு தாது | கார்பனேட் தாது | ஹேலைடு தாது | சல்பைடு தாது |
| பாக்சைட் (Al2O3.2H2O) | மார்பிள் (CaCO3) | கிரையோலைட் (Na3AlF6) | கலீனா (PbS) |
| குப்ரைட் (Cu2O) | மாக்னசைட் (MgCO3) | ஃப்ளுர்ஸ்பார் (CaF2) | இரும்பு பைரைட் (FeS2) |
| ஹேமடைட் (Fe2O3) | சிட்ரைட் (FeCO3) | பாறை உப்பு (NaCl) | ஜிங்க் ப்ளன்ட் (ZnS) |
எளிதில் கடத்தும் தன்மையன. எ.கா:வெள்ளி, தாமிரம் (டங்கஸ்டன் தவிர)
- கரையும் தன்மை: வழக்கமாக உலோகங்கள் திரவ கரைப்பான்களில் கரைவதில்லை.
வேதியியல் பண்புகள்:
இணைதிற எலக்ட்ரான்கள்: உலோக அணுக்கள் பொதுவாக 1,2 அல்லது 3 எலக்ட்ரான்களை வெளிகூட்டில் பெற்றுள்ளன.
அயனி உருவாதல் பண்பு: உலோகங்கள் எலக்ட்ரான்களை இழந்து நேர்மின் அயனிகளாக மாறும் தன்மை உடையவை. அதனால் அவை நேர்மின் சுமை பெறும்.
அயனி மின்சுமை இழத்தல்: உலோகங்களின் சேர்மங்கள் மின்னற்பகுத்தல் வினையின் போது, உலோக அயனிகள் எதிர்மின்வாய் வந்தடையும்.
அணுக்கட்டு எண்: உலோக மூலக்கூறுகள், ஆவிநிலையில், ஒற்றை அணுக்கட்டு எண்ணைப் பெற்றுள்ளன.
ஆக்சைடுகளின் தன்மை: உலோக ஆக்சைடுகள் பொதுவாக காரத்தன்மை உடையன.
அலுமினிய உலோகவியல்:
புவித்தோட்டில் மிகச் செறிந்து காணப்படும் உலோகம் அலுமினியம் ஆகும். இதன் வினைபடும் திறன் அதிகம். அதனால் சேர்ந்த நிலையில் இது காணப்படும். இதன் முக்கியத் தாதுக்கள் கீழ்க்கண்டவாறு எழுதலாம்.
| அலுமினிய தாதுக்கள் | வாய்ப்பாடு |
| பாக்சைட் | Al2O3.2H2O |
| கிரையோலைட் | Na3AlF6 |
| கொரண்டம் | Al2O3 |
அலுமினியத்தின் முக்கியத் தாது பாக்சைட் ஆகும். இத்தாதுவிலிருந்து அலுமினியம் பிரித்தெடுத்தல், 2 நிலைகளில் நடைபெறுகின்றது.
- பாக்சைட்டை அலுமினாவாக மாற்றம் செய்தல் (பேயர் முறை):
பாக்சைட்டை அலுமினாவாக மாற்றுதல் இரண்டு படிகளை உள்ளடக்கியது.
பாக்சைட் தாதுவினை, நன்கு தூளாக்கி, எரி சோடாவுடன் 1500C வெப்பநிலையில், குறிப்பிட்ட அழுத்தத்தில் வினைப்படுத்தும் போது, சோடியம் மெட்டா அலுமினேட் உருவாகிறது.
Al2O3 + 2 NaOH ???? 2 NaAlO2 + H2O
சோடியம் மெட்டா அலுமினேட்டை நீரினால் நீர்க்கச் செய்வதால், அலுமினியம் ஹைட்ராக்சைடு வீழ்படிவு உருவாகிறது.
NaAlO2 + 2 H2O ???? Al (OH)3 + NaOH
இவ்வீழ்படிவை வடிகட்டி, நன்கு கழுவி பின் 10000C வெப்பநிலையில் உலர்த்திட, அலுமினா உருவாகிறது.

- அலுமினாவை, மின்னாற்பகுத்தல் மூலம் ஒடுக்கம் செய்தல் (ஹால் முறை):
மின்னாற்பகுப்பு கலனில் உருகிய அலுமினாவை, மின்னாற்பகுப்பு முறையில் ஒடுக்கிட, அலுமினியம் கிடைக்கிறது.
அலுமினியம் எதிர்மின்வாயிலும், ஆக்ஸிஜன் நேர்மின்வாயிலும் வெளியாகிறது. வெளியாகும் ஆக்ஸிஜன், கிராபைட்டுடன் சேர்ந்து CO2 வாக மாறுகிறது.
எதிர்மின்வாய்: கிராபைட் பூசப்பட்ட இரும்புத் தொட்டி
நேர்மின்வாய்: உருகிய மின்பகுளியில் தொங்கவிடப்பட்ட கிராபைட் துண்டுகள்.
மின்பகுளி: தூய அலுமினா + உருகிய கிரையோலைட் + ஃப்ளுர்ஸ்பார் (இது மின்படுளியின் உருக்கு வெப்பநிலையைக் குறைக்கும்).
வெப்பநிலை: 9000C – 9500C
மின் அழுத்தம்: 5-6V
ஒட்டு மொத்த வினை: 2 Al2O3 ???? 4 Al + 3 O2 ↑
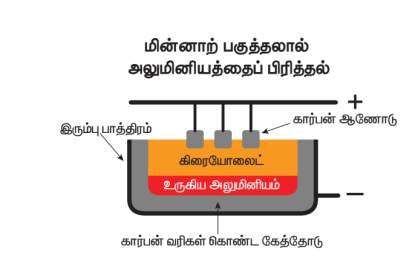
ஹால் முறை
இயற்பண்புகள்:
- இது வெள்ளியைப் போன்ற வெண்மையான உலோகம்.
- இது இலேசான, அடர்த்தி குறைந்த உலோகம்
- தகடாக அடிக்கலாம், கம்பியாக நீட்டலாம்.
- இது வெப்பத்தையும், மின்சாரத்தையும் நன்கு கடத்தும்.
- இதன் உருகுநிலை 6600C
- பளபளப்பான ஒளிரும் தோற்றம் கொண்டதாக மாற்ற இயலும்.
வேதிப்பண்புகள்:
- காற்றுடன் வினை: உலர்ந்த காற்றுடன் அலுமினியம் வினைபுரியாது. 8000C வெப்பநிலையில் அலுமினியம் காற்றுடன் வினைபுரிந்து ஆக்சைடு மற்றும் நைட்ரைடுகளை உருவாக்கும்.
4 Al + 3 O2 ???? 2 Al2 O3 (அலுமினியம் ஆக்சைடு)
2 Al + N2 ???? AIN (அலுமினியம் நைட்ரைடு)
- நீருடன் வினை: நீருடன் அலுமினியம் வினைபுரியாது. ஆனால் நீராவியுடன் செஞ்சூடேற்றிய அலுமினியம், வினைபுரிந்து அலுமினியம் ஆக்சைடுயும், ஹைட்ரஜனையும் உருவாக்குகிறது.
2 AL + 3 H2O ???? Al2O3 + 3 H2↑
(நீராவி) (அலுமினியம் ஆக்சைடு)
- காரங்களுடன் வினை: காரங்களுடன் அலுமினியம் வினைபுரிந்து அலுமினேட்களை உருவாக்குகிறது.
2 Al + 2 NaOH + 2 H2O ???? NaAlO2 + 36 H2↑
- அமிலங்களுடன் வினை: நீர்த்த மற்றும் அடர் HCl அமிலங்களுடன் அலுமினியம் வினைபுரிந்து H2 வாயுவை வெளியிடுகிறது.
2 Al + 6 HCl ???? 2 AlCl3 + 3 H2↑
அலுமினியம் குளோரைடு
அலுமினியம் நீர்த்த சல்ப்யூரிக் அமிலத்துடன் ஹைட்ரஜன் வாயுவையும், அடர் சல்ப்யூரிக் அமிலத்துடன் சல்பர்-டை-ஆக்ஸைடு வாயுவையும் வெளியிடுகிறது.
2 Al + 3 H2SO4 ???? Al2(SO4)3 + 3 H2
(நீர்த்த)
2 Al + 6 H2SO4 ???? Al2(SO4)3 + 6 H2O + 3 SO2↑
(அடர்) (அலுமினியம் சல்பேட்)
- அலுமினியம் ஒரு சிறந்த ஒடுக்கி:
அலுமினியம் பவுடரும், இரும்பு ஆக்சைடும் கொண்ட கலவையை சூடாக்கும் போது இரும்பு ஆக்சைடு இரும்பாக ஒடுக்கப்படுகின்றது. இவ்வினை அலுமினிய வெப்ப ஒடுக்க வினை ஆகும்.
Fe2O3 + 2 Al ???? 2 Fe + Al2O3 + வெப்ப ஆற்றல்
பயன்கள்:
- வீட்டுப் பாத்திரங்கள் செய்யப்பயன்படுகிறது.
- மின்கம்பி செய்யப்பயன்படுகிறது.
- விமானம் மற்றும் தொழில் இயந்திரங்களின் பாகங்களைச் செய்யப்பயன்படுகிறது.
தாமிரத்தின் உலோகவியல்:
ரோமானியர்களால், இவ்வுலோகம் குப்ரம் என்றழைக்கப்பட்டது. ஏனெனில் சைப்ரஸ் என்னும் தீவிலிருந்து எடுக்கப்பட்டதால் அவ்வாறு அழைக்கப்பட்டது. இது தனித்தும், சேர்ந்தும் காணப்படும்.
| தாமிரத்தின் தாதுக்கள் | வாய்ப்பாடு |
| காப்பர் பைரைட் | CuFeS2 |
| குப்ரைட் அல்லது ரூபி காப்பர் | Cu2O |
| காப்பர் கிளான்ஸ் | Cu2S |
காப்பரின் முக்கிய தாது காப்பர் பைரைட் ஆகும். 76 சதவீதம் தாமிரம் இத்தாதுவில் இருந்து பெறப்படுகின்றது. தாமிரம் பிரித்தெடுத்தல் கீழ்கண்டபடிகளில் நடைபெறுகிறது.
- தாதுவைச் செறிவூட்டல்: தூளாக்கப்பட்ட தாதுவானது, நுரை மிதப்பு முறையில் செறிவூட்டம் செய்யப்படுகிறது.
- வறுத்தெடுத்தல்: அடர்ப்பிக்கப்பட்ட தாதுவானது, ஆக்ஸிஜன் முன்னிலையில் வறுக்கப்படுகின்றது. அதனால் ஈரம் மற்றும் ஆவியாகும் மாசுக்களும் நீக்கப்படுகின்றன. சல்பர், பரஸ்பரஸ், ஆர்சனிக் மற்றும் ஆண்டிமனி போன்றவை ஆக்சைடுகளாக மாறி நீக்கப்படுகின்றன காப்பர் பைரைட்டானது, காப்பர், இரும்பு சல்பைடுகளாக பகுதியளவு மாறுகிறது.
- CuFeS2 + Cu2S + 2 FeS + SO2↑
- உருக்கிப்பிரித்தல்: வறுக்கப்பட்ட தாதுவானது தூளாக்கப்பட்ட கார்பன் மற்றும் மணலுடன் கலந்து சூடேற்றும் போது மாட்டியும், (Cu2S + FeS) கசடும் உருவாகும். கசடை நீக்க வேண்டும்.
- பெஸ்ஸிமராக்குதல்: உருகிய மாட்டியை பெஸ்ஸிமர் மாற்று உலையிலிட்டு சூடேற்றும் போது கொப்புளக் காப்பர் உருவாகும். மாட்டியில் உள்ள இரும்பு சல்பைடு ஆக்ஸிஜேற்றம் அடைந்து இரும்பு ஆக்சைடாக மாறுகிறது. இவை சிலிகாவுடன் சேர்ந்து கசடாக மாறும்.
2 FeS + 3 O2 ???? 2 FeO + 2 SO2↑
FeO + SiO2 ???? FeSiO3 (கசடு) (இரும்பு சிலிகேட்)
2 Cu2S + 3O2 ???? 2 Cu2O + 2 SO2 ↑
2 Cu2O + Cu2S ???? 6 Cu + SO2 (கொப்புள காப்பர்)
- தூய்மையாக்கல்: 98% காப்பரும், 2% மாசுக்களும் உள்ள கொப்புளக் காப்பரை மின்னாற்பகுத்தல் செய்வதன் மூலம் மிகத் தூய்மையான உலோகம் பெறலாம்.
மின்னாற்பகுத்தல் முறையில் தூய்மை
எதிர்மின்வாய்: தூய மெல்லிய காப்பர் தகடு.
நேர்மின்வாய்: மாசு கலந்த காப்பர்.
மின்பகுளி: கந்தக அமிலம் கலந்த காப்பர் சல்பேட் மின்பகுளியின் வழியாக மின்சாரத்தைச் செலுத்தும்போது தூய எதிர்மின் முனையிலும், மாசுக்கள் நேர்மின் முனையிலும் படிகின்றன. நேர்மின் வாயின் அடியில் படியும் மாசுக்கள் ஆனோடு மண் எனப்படும்.
தாமிரத்தின் இயற்பண்புகள்: இது செம்பழுப்பு நிறமுள்ள உலோகம் ஆகும். பளபளப்பும், அதிக அடர்த்தியும் கொண்டது. இதன் உருகுநிலை 13560C.
தாமிரத்தின் வேதிப்பண்புகள்:
- காற்றுடனும், ஈரப்பதத்துடனும் வினை: தாமிரம் CO2 மற்றும் ஈரப்பதத்துடன் வினைபுரிந்து, பச்சை நிறக் காப்பர் கார்பனேட் படலத்தை உருவாக்குகிறது.
2 Cu + O2 + CO2 + H2O ???? CuCO3.Cu(OH)2
- வெப்பத்துடன் வினை: வெவ்வேறு வெப்பநிலைகளில், தாமிரம், ஆக்ஸிஜனுடன், வினைபுரிந்து இருவேறு ஆக்சைடுகளை உருவாக்கும். CuO, Cu2O.

- அமிலங்களுடன் வினை:
அ. நீர்த்த HCl மற்றும் H2SO4 உடன் வினை காற்றில்லா சூழ்நிலையில், நீர்த்த HCL மற்றும் H2SO4 அமிலங்களுடன் வினை புரியாது. ஆனால் காற்றின் முன்னிலையில் அமிலத்தில் கரைகின்றது.
2 Cu + 4 HCl + O2 காற்று ???? 2 CuCl2 + 2 H2O
Cu + 2 H2SO4 ???? CuSO4 + SO2↑ + 2 H2O
ஆ. நீர்த்த HNO3 உடன் வினை:
நீர்த்த HNO3 உடன் வினைபுரிந்து நைட்ரிக் ஆக்ஸைடு வாயுவை வெளியேற்றுகின்றது.
3 Cu + 8 HNO3 ???? 3 Cu(NO3)2 + 2 No ↑ + 4 H2O
- குளோரினுடன் வினை:
தாமிரம், குளோரினுடன் வினைபுரிந்து காப்பர் (II) குளோரைடை தருகின்றது.
Cu + Cl2 ???? CuCl2
- காரத்துடன் வினை:
தாமிரம் காரத்தினால் எந்த பாதிப்பும் அடைவதில்லை.
பயன்கள்:
- மின்கம்பிகளையும், மின் உபகரணங்களையும் உருவாக்கப் பயன்படுகிறது.
- கலோரி மீட்டர், பாத்திரங்கள், நாணயங்கள் போன்றவற்றை உருவாக்கப் பயன்படுகிறது.
- மின்முலாம் பூசப் பயன்படுகிறது.
- தங்கம் மற்றும் வெள்ளியோடு கலந்து, உலோகக் கலவையாக்கி நாணயங்கள் மற்றும் அணிகலன்கள் உருவாக்கப் பயன்படுகிறது.
இரும்பின் உலோகவியல்:
கிடைக்கும் பாங்கு: அலுமினியத்திற்கு அடுத்து, மிக அதிகமாக காணப்படும் உலோகம் இரும்பு ஆகும். இயற்கையில், இது ஆக்சைடு, சல்பைடு மற்றும் கார்பனேட்டுகளாக கிடைக்கின்றன. இரும்பின் தாதுக்களாவன.
| இரும்பின் தாதுக்கள் | வாய்ப்பாடு |
| ஹேமடைட் | Fe22O3 |
| மேக்னடைட் | Fe3O4 |
| இரும்பு பைரைட் | FeS2 |
இரும்பின் முக்கிய தாது ஹேமடைட் (Fe2O3) ஆகும்.
- புவியீர்ப்பு முறையில் அடர்ப்பித்தல்: தூளாக்கப்பட்ட தாதுவை, சீராக ஓடும் நீரில் கழுவும்போது லேசான மாசுக்கள் அகற்றப்பட்டு, கனமான தாதுக்கள் கீழே படிகின்றன.
- காற்றுள்ள மற்றும் காற்றில்லா சூழலில் வறுத்தல்: அடர்ப்பிக்கப்பட்ட தாதுவானது, அளவான காற்றில் உலையில் சூடேற்றப்படும் போது, ஈரப்பதம் வெளியேறி சல்பர், ஆர்சனிக் மற்றும் பாஸ்பரஸ் மாசுக்கள் ஆக்ஸிஜனேற்றம் அடைகின்றன.
- ஊது உலையில் உருக்கிப்பிரித்தல்: வறுக்கப்பட்ட தாது, கல்கரி, சுண்ணாம்புக்கல் இவற்றை 8:4:1 என்ற விகிதத்தில் எடுத்துக் கொண்டு, உலையின் மேலுள்ள கிண்ணக்கூம்பு அமைப்பு வழியாக, செலுத்தப்படுகிறது. உலையில் மூன்று முக்கிய பகுதிகள் உள்ளன.
அ. கீழ்ப்பகுதி (எரிநிலை மண்டலம்):
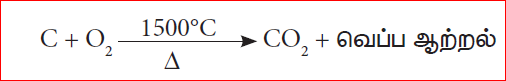
இந்தப் பகுதியின் வெப்பநிலை 15000Cஆகும். வெப்பக்காற்றுடன் தாதுக்கலவை சேரும் போது, ஆக்ஸிஜனுடன் எரிந்து CO2 வாக மாறுகிறது.
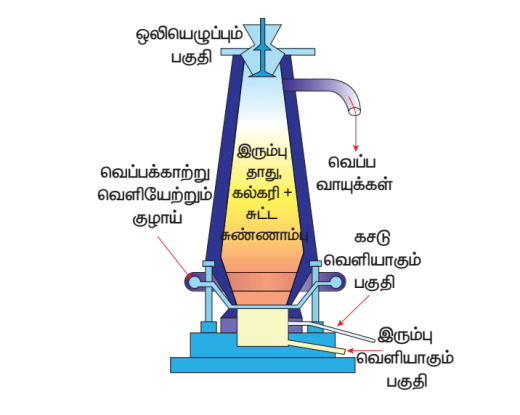
ஊது வெப்ப உலை
இவ்வினையிலிருந்து வெப்ப ஆற்றல் வெளியாவதால் வெப்ப உமிழ்வினை எனப்படும்.
நடுப்பகுதி அல்லது உருக்கு மண்டலம்:
இப்பகுதி 10000C வெப்பநிலையில் உள்ளது. இங்கு CO2 ஆனது CO ஆக ஓடுக்கமடைகிறது.
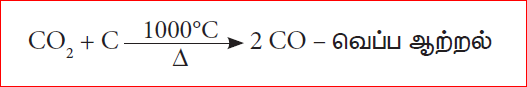
சுண்ணாம்புக்கல் சிதைந்து, கால்சியம் ஆக்சைடையும், CO2 வையும் தரும்.
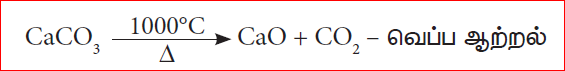
மேற்கண்ட இருவினைகளில், வெப்பம் உட்கவரப்படுவதால் வெப்ப கொள்வினைகள் ஆகும். கால்சியம் ஆக்சைடு மணலுடன் சேர்ந்து கால்சியம் சிலிகேட் எனும் கசடாகிறது.
CaO + SiO2 ???? CaSiO3
மேற்பகுதி (ஒடுக்கும் மண்டலம்):
இப்பகுதியில் 4000C வெப்பநிலையில் ஃபெரிக் ஆக்சைடு, கார்பன் மோனக்சைடு மூலம் இரும்பாக ஒடுக்கம் அடைகிறது.
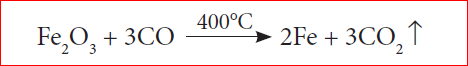
கசடை நீக்கிய பிறகு, உருகிய இரும்பானது, உலையின் அடியில் சேகரிக்கப்படுகிறது. இவ்விரும்பு மீண்டும் உருக்கப்பட்டு விதவித அச்சுக்களில் வார்க்கப்படுவதால், இது வார்ப்பிரும்பு எனப்படும்.
இயற்பண்புகள்:
- இது ஒரு பளபளப்பான உலோகம், சாம்பல் வெள்ளை நிறமுடையது.
- இழுவிசை, தகடாக்கும் தன்மை மற்றும் கம்பியாக்கும் தன்மையைப் பெற்றிருக்கும்.
- காந்தமாக மாற்ற இயலும்.
வேதிப்பண்புகள்:
- காற்றுடன் வினை: இரும்பு, காற்றுடன் சூடேற்றும் போது வினைபுரிந்து இரும்பு ஆக்சைடு உருவாகிறது.
3 Fe + 2O2 ???? Fe3O4 (கறுப்பு நிறம்)
- ஈரக்காற்றுடன் வினை: இரும்பானது ஈரக்காற்றுடன் வினைபுரிந்து பழுப்பு நிற, நீரேறிய பெர்ரிக் ஆக்சைடை உருவாக்குகின்றது. இச்சேர்மமே துரு எனப்படும். இந்நிகழ்ச்சி துருபிடித்தல் எனப்படும்.
4 Fe + 3O2 + x H2O ???? 2 Fe2O3 . x H2O (துரு)
- நீராவியுடன் வினை: செஞ்சூடெற்றிய இரும்பின் மீது, நீராவியை பாய்ச்சும் போது மேக்னட்டிக் ஆக்சைடு உருவாகிறது.
3 Fe + F H2O (நீராவி) ???? Fe3 O4 + 4 H2 ↑
- குளோரினுடன் வினை: இரும்பு குளோரினுடன் சேர்ந்து ஃபெரிக்குளோரைடு உருவாகிறது.
2 Fe + 3 Cl2 ???? 2 FeCl3 (ஃபெரிக்குளோரைடு)
- அமிலங்களுடன் வினை: நீர்த்த HCl மற்றும் H2SO4 அமிலங்களுடன் இரும்பு வினைபுரிந்து, H2 வாயுவை வெளியேற்றுகின்றது.
Fe + 2 HCl ???? FeCl2 + H2 ↑
Fe + H2SO4 ???? FeSO4 + H2 ↑
நீர்த்த நைட்ரிக் அமிலத்துடன், இரும்பு குளிர்ந்த நிலையில் வினைபுரிந்து பெரஸ் நைட்ரேட் மற்றும் அம்மோனியம் நைட்ரேட்டை உருவாக்குகின்றது.
4 Fe + 10 HNO3 ???? 4 Fe (NO3)2 + NH4 NO3 + 3 H2O
அடர்கந்தக அமிலத்துடன், இரும்பு வினைபுரிந்து ஃபெரிக் சல்பேட்டை உருவாக்குகின்றது.
2 Fe + 6 H2SO4 ???? Fe2 (SO4)3 + 3 SO2 + 6 H2O
அடர் நைட்ரிக் அமிலத்தில், இரும்பை அமிழ்த்தும் போது இரும்பு ஆக்ஸைடு படலம் உருவாவதால், இரும்பு தன் திறனை இழக்கின்றது.
இரும்பின் வகைகள் மற்றும் பயன்கள்:
வார்ப்பிரும்பு (2% – 4.5% கார்பன் உடைய இரும்பு) ஸ்டவ்கள், கழிவு நீர்க் குழாய்கள், ரேடியேட்டர்கள், கழிவு நீர் சாக்கடை மூடிகள் இரும்பு வேலிகள் ஆகியவற்றை உருவாக்கப் பயன்படுகிறது.
எஃகு (0.25% – 2% கார்பன் உடைய இரும்பு) கட்டிடக் கட்டுமானங்கள், எந்திரங்கள் மின்கடத்து கம்பிகள், T.V கோபுரங்கள் மற்றும் உலோகக் கலவைகள் ஆகியவற்றை உருவாக்கப் பயன்படுகிறது.
தேனிரும்பு (< 0.25% கார்பன் உடைய இரும்பு) கம்பிச்சுருள், மின்காந்தங்கள் மற்றும் நங்கூரம் இவற்றை செய்யப்பயன்படுகிறது.
உலோகக் கலவைகள்:
இரண்டு அல்லது அதற்கு மேற்பட்ட உலோகங்கள் அல்லது உலோகங்களும், அலோகங்களும் சேர்ந்த ஒரு படித்தான கலவையே உலோகக்கலவை ஆகும்.
உலோகக் கலவையின் பண்புகள், அதன் உள் அடங்கிய உலோகத்தின் பண்புகளிலிருந்து மாறுபடும். தூய தங்கம் மிக மென்மையான உலோகம். அதோடு சிறிதளவு காப்பரைச் சேர்க்கும் போது, வலிமையும், பயன்பாடும் அதிகரிக்கின்றது.
இரசக்கலவை:
இரசக்கலவை என்பது பாதரசத்துடன், உலோகம் சேர்ந்த கலவையாகும். எலக்ட்ரான்களுக்கும், நேர்மின்சுமை கொண்ட உலோக அயனிகளுக்கும் இடைப்பட்ட நிலைமின் கவர்ச்சி விசையால், விளையும் உலோகப் பிணைப்பின் மூலம் இக்கலவைகள் உருவாகின்றன. எ.கா:சில்வர் டின் ரசக்கலவை. இது பற்குழிகள் அடைக்கப்பயன்படுகிறது.
உலோகக் கலவை உருவாக்குவதற்ககான காரணங்கள்:
- நிறம் மற்றும் வடிவங்களை மாற்றியமைக்க.
- வேதிப்பண்புகளை மாற்றியமைக்க.
- உருகுநிலையைக் குறைக்க.
- கடின தன்மை மற்றும் இழுவிசையை அதிகரிக்க.
- மின்தடையை அதிகரிக்க.
உலோகக் கலவைகளை உருவாக்கும் முறைகள்:
அ. உலோகங்களை உருக்கிச் சேர்த்தல்:
எ.கா.ஜிங்க் மற்றும் காப்பரை உருக்கிச் சேர்த்தல் மூலம் பித்தளை உருவாகிறது.
ஆ. நன்கு பகுக்கப்பட்ட உலோகங்களை அழுத்தி சேர்த்தல்:
எ.கா: மர உலோகம் இது காரீயம், வெள்ளீயம், பிஸ்மத், மற்றும் காட்மியம் தூள் போன்றவற்றை உருக்கிச் சேர்த்த கலவையாகும்.
திடக்கரைசல்களான உலோகக் கலவை: உலோகக் கலவையை திடக்கரைசல் என்று கூறலாம். இதில், செறிவு நிறைந்துள்ள உலோகம் கரைப்பான் ஆகும். மற்ற உலோகங்கள் கரைபொருள் எனப்படும்.
எ.கா பித்தளை என்ற உலோகக் கரைசலில் ஜிங்க் என்பது கரைபொருள்: காப்பர் என்பது கரைப்பான் ஆகும்.
உலோகக் கலவைகளின் வகைகள்:
இரும்பின் பங்கைப் பொறுத்து உலோகக் கலவையை இரண்டாகப் பிரிக்கலாம்.
ஃபெரஸ் உலோகக் கலவை: இதில் இரும்பு முக்கியப் பங்களிக்கிறது. எ.கா:துருப்பிடிக்காத இரும்பு, நிக்கல் இரும்பு கலவை.
ஃபெரஸ் இல்லா உலோகக் கலவை: இதில் இரும்பின் முக்கிய பங்களிப்பு இல்லை. எ.கா:அலுமினியக் கலவை, காப்பர் கலவை.
காப்பர் கலவை (இரும்பு அற்றது)
| கலவைகள் | பயன்கள் |
| பித்தளை (Cu, Zn) | மின் இணைப்புகள், பதக்கங்கள் அலங்காரப் பொருட்கள், கடின உபகரணங்கள் |
| வெண்கலம் (Cu, Sn) | சிலைகள், நாணயங்கள், அழைப்பு மணிகள் |
அலுமினியக் கலவை (இரும்பு அற்றது)
| கலவைகள் | பயன்கள் |
| டியுராலுமின் (Al, Mg, Mn, Cu) | விமானத்தின் பகுதிகள், ப்ரஷர் குக்கர்கள் |
| மெக்னலியம் (Al, Mg) | விமானத்தின் பகுதிகள், அறிவியல் உபகரணங்கள் |
இரும்புக் கலவைகள்
| கலவைகள் | பயன்கள் |
| துருப்பிடிக்காத இரும்பு (Fe,C, Ni, Cr) | பாத்திரங்கள் வெட்டும் கருவிகள், வாகன உதிரிபாகங்கள் |
| நிக்கல் இரும்பு (Fe, C, Ni) | கம்பிகள் விமானத்தின் உதிரிப் பாகங்கள், உந்திகள் |
உலோக அரிமானம்:
வேதிவினைகள் அல்லது மின் வேதி வினைகள் மூலம் சுற்றுச் சூழலோடு வினைபுரிந்து படிப்படியாக நடக்கும் உலோகத்தின் சிதைவே, உலோக அரிமானம் ஆகும். இது ஒரு இயற்கை நிகழ்வு. இதில் உலோகமானது, ஆக்சைடு, ஹைட்ராக்சைடு அல்லது சல்பைடாக மாறி தன் உலோகத் தன்மையை இழக்கிறது.
துரு என்பது நீரேறிய ஃபெரிக் ஆக்சைடு Fe2O3 . xH2O என வேதியியல் முறையில் அழைக்கப்படும். துருப்பிடித்தல் ஆனது. இரும்பின் புறப்பரப்பில், செம்பழுப்பு நிற நீரேறிய ஃபெரிக் ஆக்சைடை உருவாக்குகின்றது.
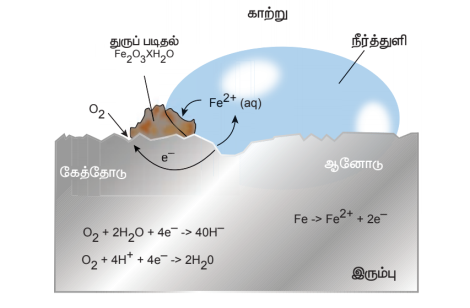
துருப்பிடித்தல்
உலோக அரிமானத்தின் வகைகள்:
- உலர் அரிமானம் (அல்லது) வேதிமுறை அரிமானம்:
ஈரப்பதம் இல்லா நிலையில், நடைபெறும் அரிமானச் செயல் உலர் அரிமானம் ஆகும். இந்நிகழ்வில் அரிக்கும் திரவங்கள் அல்லது வாயுக்களான O2, N2, SO2, H2S ஆகியவை அதிக வெப்ப நிலையில் உலோகத்தின் மேல் வேதிவினைபுரிந்து மாற்றம் நடைபெறுகின்றது. இவை அனைத்திலும் O2வானது வேதியியல் முறைப்படி அதிக அளவில் வினைபுரியும் வாயுவாக செயல்படுகிறது.
- ஈரநிலை அரிமானம் (அல்லது) மின்வேதியியல் நிலை அரிமானம்:
ஈரப்பதத்தால் நடைபெறும் அரிமான நிகழ்வு, ஈரநிலை அரிமானம் ஆகும். உலோகமானது, நீருடன் அல்லது உப்புக்கரைசலுடன் அல்லது அமில, காரங்களுடன் மின் வேதிவினை புரிந்து அரிமானத்தை உருவாக்கும்.
அரிமானத்தைத் தடுக்கும் முறைகள்:
- உலோகக் கலவையாக்கல்:
உலோகங்களை ஒன்றோடொன்று கலந்து கலவையாக்கல் மூலம், அரிமானத்தை தடுக்கலாம். எ.கா:துருப்பிடிக்காத இரும்பு.
- புறப்பரப்பை பூசுதல்:
உலோகத்தின் மீது பாதுகாப்புக் கலவை பூசுதல் அரிமானத்தை தடுக்கும். இதன் வகைகளாவன.
அ. நாகமுலாம் பூசுதல்: இரும்பின் மீது துத்தநாக மின் முலாம் பூசுவதற்கு நாகமுலாம் பூசுதல் என்று பெயர்.
ஆ. மின் முலாம் பூசுதல்: ஒரு உலோகத்தை மற்றொரு உலோகத்தின் மேல், மின்சாரத்தின் மூலம் பூசுதல் மின்முலாம் பூசுதல் ஆகும்.
இ. ஆனோட்டாக்கல்: உலோகத்தின் புறப்பரப்பை, மின் வேதிவினைகளின் மூலம், அரிமான எதிர்புள்ளதாய் மாற்றும் நிகழ்வு ஆனோடாக்கல் ஆகும். அலுமினியம் இந்த முறைக்கு பயன்படுகிறது.
ஈ.கேத்தோடு பாதுகாப்பு: எளிதில் அரிமானம் அடையும் உலோகத்தை ஆனோடாகவும், பாதுகாக்க வேண்டிய உலோகத்தைக் கேத்தோடாகவும் கொண்டு, மின் வேதி வினைக்கு உட்படுத்தும் நிகழ்வு கேத்தோடு பாதுகாத்தல் ஆகும். இவ்வினையில் எளிதில் அரிபடும் உலோகம் தியாக உலோகம் எனப்படும்.
பாம்பன் பாலம்:
இராமேஸ்வரத்தின் பாம்பன் தீவையும், இந்தியாவின் பெரும் நிலப்பரப்பையும் இணைக்கும் ரயில் பாலமே பாம்பன் பாலமாகும். 1914ல் இந்தியாவில் திறக்கப்பட்ட முதல் கடல்பாலம் என்ற பெருமை இதற்கு உண்டு. 2010ஆம் ஆண்டு திறக்கப்பட்ட பந்த்ராவலி என்ற கடற்பாலம் நீளமானது. இப்பாம்பன் பாலத்தில் ஏற்படும் உலோக அரிமானமானது. குறிப்பிட்ட கால இடைவெளியில் கம்பிகளுக்கு அடிக்கப்படும் உலோக அரிமானத்தைத் தடுக்கும் சிறப்பு வண்ணப் பூச்சுகள் மூலம் தடுக்கப்படுகிறது, மேலும் இது நம் வரலாற்றில் நினைவுச் சின்னமாகப் பாதுகாக்கப்படுகிறது.

பாம்பன் பாலம்
நினைவில் கொள்க:
- நவீன ஆவர்த்தன விதி: தனிமங்களின் இயல் மற்றும் வேதியல் பண்புகள் அவற்றின் அணு எண்களின் சார்பாக அமையும்.
- தனிமங்களை சீரான முறையில, தொகுதிகளாகவும், தொடர்களாவும், வரிசையாகக் கொண்ட அட்டவணை தனிம வரிசை அட்டவணை ஆகும்.
- நன்கு வறுத்த உலோக ஆக்சைடை உலோகமாக உருக்கி ஒடுக்கும் முறை உருக்கி பிரித்தல் ஆகும்.
- நீர்த்த மற்றும் அடர் நைட்ரிக் அமிலம் அலுமினிய உலோகத்துடன் வினைபுரியாது. பரப்பில் உருவாகும் ஆக்சைடு படலமே இதன் காரணம்.
- இரும்பை அதன் தாதுவிலிருந்து பிரித்தெடுக்க தேவையானவை, வறுத்தெடுக்கப்பட்ட தாது, கரி, சுண்ணாம்புக்கல் முறையே 8:4:1 என்ற விகிதத்தில் ஆகும்.
- தாமிரப் பாத்திரம் மீது ஈரக்காற்றுபடுவதால், அதன் புறப்பரப்பில் பச்சைநிற படலம் ஆனது கார காப்பர் கார்பனேட்டால் உருவாகிறது.
- உலோகக் கலவை என்பது இரண்டு அல்லது அதற்கு மேற்பட்ட உலோகங்களின் ஒருபடித்தான கலவையாகும்.
- இரசக்கலவை என்பது உலகமும், பாதரசமும் கலந்த கலவையாகும். எ.கா:Ag-Sn இரசக்கலவையானது பற்குழிகளை அடைக்கப்பயன்படுகிறது.
- துருவின் வேதிப்பெயர் நீரேறிய ஃபெரிக் ஆக்சைடு ஆகும். அதன் சமன்பாடு Fe2O3.xH2O.
உங்களுக்கு தெரியுமா?
மந்த வாயுக்கள் எலக்ட்ரான்களை ஏற்கும் தன்மையற்றவை. ஏனெனில், அவற்றின் வெளிமட்டத்தில் உள்ள S மற்றும் P ஆர்பிட்டால்கள் முழுமையாக எலக்ட்ரான்களால் நிரம்பி உள்ளவை. அதனால் மேலும் ஒரு எலக்ட்ரானை சேர்ப்பது இயலாது. எனவே இவற்றின் எலக்ட்ரான் நாட்டம் பூஜ்ஜிய மதிப்பை பெறுகின்றன.
உலோக ஆக்சைடிலிருந்து உலோகத்தைப் பிரித்தல் 3 வகைப்படும்.
| அதிவினைபடும் உலோகங்கள் | சாதாரணமாக வினைபடும் உலோகங்கள் | குறைவாக வினைபடும் உலோகங்கள் |
| Na, K, Ca, Mg, Al | Zn, Fe, pb, Cu | Ag, Hg |
| உலோக ஆக்சைடு உலோகமாக மின்னாற்பகுப்பின் மூலம் ஒடுக்கம் அடைகிறது. | உலோக ஆக்சைடு உலோகமாக கார்பன் (CoKe) உதவியுடன் வேதி ஒடுக்கம் அடைகிறது | செஞ்சூடேற்றி சிதைவுறுதலால் உலோக ஆக்சைடு உலோகமாக ஒடுக்கம் அடைகிறது. |
நீர்த்த மற்றும் அடர் நைட்ரிக் அமிலம் அலுமினியத்தோடு வினைபுரிவதில்லை. மாறாக அலுமினியத்தின் மேல் ஆக்சைடு படலம் உருவாவதால், அதன் வினைபடும் திறன் தடுக்கப்படுகிறது.