அமிலங்கள் மற்றும் காரங்கள் Notes 8th Science Lesson 19 Notes in Tamil
அமிலங்கள் மற்றும் காரங்கள் Notes 8th Science Lesson 19 Notes in Tamil
அறிமுகம்:
நம் அன்றாட வாழ்வில் பல்வேறு உணவுப் பொருள்களைப் பயன்படுத்துகிறோம். புளி, திராட்சை, எலுமிச்சை, தயிர் போன்ற உணவுப்பொருள்கள் புளிப்புச் சுவையுடையவை. இவற்றை அமிலத்தன்மை வாய்ந்தவை என்கிறோம். சோடியம் பைகார்பனேட், சோப்பு போன்றவை கசப்புச் சுவை உடையவை. இவற்றை காரத்தன்மை உடையவை என்கிறோம். இது இப்பொருள்கள் அமிலம் அல்லது காரத்தைக் கொண்டிருக்கின்றன என்பதைக் குறிக்கிறது. ஆனால், அமிலங்கள் மற்றும் காரங்கள் என்றால் என்ன? அமிலங்கள் மற்றும் காரங்கள் என்பவை வேதியியல் சேர்மங்களின் ஒரு முக்கியமான பிரிவாகும். அவை அறிவியலின் ஒவ்வொரு துறையிலும் குறிப்பிடத்தக்க பங்கைக் கொண்டுள்ளன. நாம் குளியலுக்குப் பயன்படுத்தும் சோப்பு முதல் சமையலறையில் உள்ள வினீகர் வரை அனைத்திலும் அமிலங்கள் மற்றும் காரங்கள் உள்ளன. இவை உயிரியல், தொழிற்சாலை, சுற்றுச்சூழல் ஆகிய அனைத்திலும் முக்கியமானவை. எடுத்துக்காட்டாக, நாம் பயன்படுத்தும் ஆஸ்பிரின் என்ற வலி நிவாரணி ஒரு அமிலமாகும். அமில நீக்கியாகப் பயன்படும் மருந்து ஒரு காரமாகும். இது போலவே, பல்வேறு உயிரியல் மூலக்கூறுகள் அமிலங்களாகவோ அல்லது காரங்களாகவோ உள்ளன. நாம் உண்ணும் உணவில் உள்ள கொழுப்புகளில் அமிலங்களும், செல்லின் அடிப்படைப் பொருள்களான டி.என்.ஏ வில் காரங்களும் உள்ளன. இந்தப் பாடத்தில் அமிலங்கள் மற்றும் காரங்களின் பண்புகள், பயன்கள், அவற்றிற்கு இடையேயான நடுநிலையாக்கல் வினைகள் மற்றும் நிறங்காட்டிகள் பற்றி காண்போம்.
அமிலங்கள்:
அமிலம் என்ற சொல்லானது புளிப்பு எனப் பொருள்படும் ‘அசிடஸ்’ என்ற இலத்தீன் மொழிச் சொல்லில் இருந்து வருவிக்கப்பட்டது. எனவே, புளிப்புச் சுவை கொண்ட வேதிச்சேர்மங்கள் பொதுவாக அமிலங்கள் எனப்படுகின்றன. அனைத்து அமிலங்ளும் ஒன்று அல்லது அதற்கு மேற்பட்ட இடப்பெயர்ச்சி செய்யத்தக்க ஹைட்ரஜன் அணுக்களைப் பெற்றுள்ளன. மேலும், அவற்றை நீரில் கரைக்கும்பொழுது ஹைட்ரஜன் அயனிகளை (H+) அவை வெளியிடுகின்றன. எடுத்துக்காட்டாக, ஹைட்ரோகுளோரிக் அமிலம் (HCI), சல்பியூரிக் அமிலம் (H2SO4) மற்றும் நைட்ரிக் அமிலம் (HNO3) ஆகியவற்றை நீரில் கரைக்கும் பொழுது ஹைட்ரஜன் அயனிகளை (H+) அவை கொடுக்கின்றன.
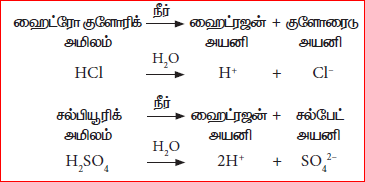
எனவே, நீரில் கரையும்போது ஹைட்ரஜன் அயனிகளை வெளியிடும் வேதிச்சேர்மங்கள் அமிலங்கள் என வரையறுக்கப்படுகின்றன.
அமிலங்களை அவற்றின் மூலங்களைப் பொருத்து கரிம மற்றும் கனிம அமிலங்கள் என வகைப்படுத்தலாம். சில அமிலங்கள் பழங்கள் மற்றும் காய்கறிகளில் காணப்படுகின்றன. இவை கரிம அமிலங்கள் எனப்படும். எ.கா. சிட்ரிக் அமிலம், டார்டாரிக் அமிலம்.
கரிம அமிலங்கள் மற்றும்அவை உள்ள பொருள்கள்
| அமிலத்தின் பெயர் | உணவுப்பொருள் |
| சிட்ரிக் அமிலம் | ஆரஞ்சு |
| லாக்டிக் அமிலம் | தயிர் |
| ஆக்சாலிக் அமிலம் | தக்காளி |
| அசிட்டிக் அமிலம் | வினிகர் |
| மாலிக் அமிலம் | ஆப்பிள் |
| டார்டாரிக் அமிலம் | புளி |
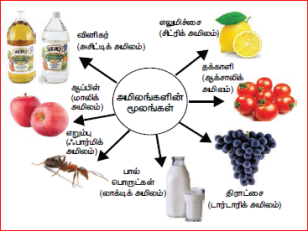
அமிலங்கள் உள்ள உணவுப்பொருள்கள்
மாறாக, தொழிற்சாலைகளில் அமிலங்கள் செயற்கையாக உற்பத்தி செய்யப்படுகின்றன. இந்த அமிலங்கள் கனிம அமிலங்கள் எனப்படும். எ.கா. ஹைட்ரோகுளோரிக் அமிலம் (HCl), சல்பியூரிக் அமிலம் (H2SO4) நைட்ரிக் அமிலம் (HNO3). அமிலங்களை மேலும் பலவகையாக வகைப்படுத்த இயலும். அவற்றைப் பற்றி நீங்கள் உயர் வகுப்புகளில் கற்க இருக்கிறீர்கள்.
அமிலங்களின் பண்புகள்:
அ. இயற்பியல் பண்புகள்:
- அமிலங்கள் புளிப்புச் சுவை கொண்டவை.
- அமிலங்கள் நிறமற்றவை.
- அமிலங்கள் அரிக்கும் தன்மை கொண்டவை. மேலும், வலிமையான அமிலங்கள் மனிதர்களின் தோல், துணி மற்றும் காகிதத்தைப் பாதிக்கின்றன.
- பொதுவாக அமிலங்கள் திரவ நிலையில் காணப்படும். ஒரு சில அமிலங்கள் திண்ம நிலையிலும் உள்ளன. எ.கா. பென்சாயிக் அமிலம்.
- அமிலங்கள், நிறங்காட்டிகளின் நிறத்தை மாற்றுகின்றன. நீல லிட்மஸ் தாளை சிவப்பாகவும், மெத்தில் ஆரஞ்சு கரைசலை சிவப்பாகவும் மாற்றுகின்றன.
- அமிலங்கள் நீரில் நன்கு கரைகின்றன.
- அமிலங்களின் நீர்க் கரைசல் மின்சாரத்தைக் கடத்துகிறது.
பென்சாயிக் அமில படிகம்
ஆ. வேதியியல் பண்புகள்:
- உலோகங்களுடன் வினை:
துத்தநாகம், மெக்னீசியம், அலுமினியம் மற்றும் இரும்பு போன்ற உலோகங்கள் ஹைட்ரோகுளோரிக் அமிலம் மற்றும் சல்பியூரிக் அமிலத்துடன் (கந்தக அமிலம்) வினைபுரிந்து உலோக உப்புகளையும் ஹைட்ரஜன் வாயுவையும் தருகின்றன.
உலோகம் + நீர்த்த அமிலங்கள் ???? உலோக உப்பு + ஹைட்ரஜன் வாயு
எடுத்துக்காட்டு:
துத்தநாகம் + ஹைட்ரோ குளோரிக் அமிலம் ???? துத்தநாக குளோரைடு + ஹைட்ரஜன் வாயு
Zn + 2HCl ???? ZnCl2 + H2↑
இரும்பு + சல்பியூரிக் அமிலம் ???? இரும்பு சல்பேட் + ஹைட்ரஜன் வாயு
Fe + H2SO4 ???? FeSO4 + H2↑
- உலோக கார்பனேட்டுகள் மற்றும் பைகார்பனேட்டுகளுடன் வினை:
நீர்த்த அமிலங்களுடன் உலோக கார்பனேட்டுகள் மற்றும் பைகார்பனேட்டுகள் வினைபுரியும்போது கார்பன் டைஆக்சைடு வாயுவும், நீரும் உருவாகின்றன. எடுத்துக்காட்டாக, கால்சியம் கார்பனேட்டானது சல்பியூரிக் அமிலத்துடன் வினைபுரிந்து கால்சியம் சல்பேட், கார்பன் டை ஆக்சைடு மற்றும் நீரைக் கொடுக்கிறது.
கால்சியம் கார்பனேட் + நீர்த்த சல்பியூரிக் அமிலம் ???? கால்சியம் சல்பேட் + கார்பன் டை ஆக்சைடு + நீர்
CaCO3 + H2SO4 ???? CaSO4 + CO2 + H2O
- உலோக ஆக்சைடுகளுடன் வினை:
பல்வேறு உலோக ஆக்சைடுகள் நீர்த்த அமிலங்களுடன் வினைபுரிந்து அவற்றின் உலோக உப்புகள் மற்றும் நீரைத் தருகின்றன.
உலோக ஆக்சைடுகள் + நீர்த்த அமிலம் ???? உலோக உப்புகள் + நீர்
எடுத்துக்காட்டு:
கால்சியம் ஆக்சைடு + ஹைட்ரோ குளோரிக் அமிலம் ???? கால்சியம் குளோரைடு + நீர்
CaO + 2HCl ???? CaCl2 + H2O
அமிலங்களின் பயன்கள்:
- நமது வயிற்றில் சுரக்கும் ஹைட்ரோ குளோரிக் அமிலம் உணவுப்பொருள்களின் செரிமானத்திற்கு உதவுகிறது.
- உணவுப்பொருள்கள் கெட்டுப்போகாமல் இருக்க வினிகர் (அசிட்டிக் அமிலம்) பயன்படுத்தப்படுகிறது.
- ஊறுகாய் போன்ற உணவுப் பொருள்கள் கெட்டுப்போகாமல் இருக்க பென்சாயிக் அமிலம் பயன்படுத்தப்படுகிறது.
- குளியல் சோப்புகள் மற்றும் சலவை சோப்புகள் தயாரிக்க உயர் கொழுப்பு அமிலங்களின் சோடியம் உப்புகள் அல்லது பொட்டாசியம் உப்புகள் பயன்படுகின்றன.
- சல்பியூரிக் அமிலம் வேதிப்பொருள்களின் அரசன் என்று அழைக்கப்படுகிறது. இது மிகச் சிறந்த நீர் நீக்கியாகச் செயல்படுகிறது. இது பல்வேறு வகையான சலவை சோப்புகள், வண்ணப்பூச்சுகள் (பெயிண்ட்கள்), உரங்கள் மற்றும் பல வேதிப்பொருள்கள் தயாரிக்கும் தொழிற்சாலைகளில் பயன்படுத்தப்படுகிறது.
- ஹைட்ரோகுளேரிக் அமிலம், நைட்ரிக் அமிலம் மற்றும் சல்பியூரிக் அமிலம் போன்றவை முக்கியமான ஆய்வகக் காரணிகளாகச் செயல்படுகின்றன.

அமிலங்களின் பயன்கள்
- அனைத்து உயிரினங்களின் செல்களும் நியூக்ளிக் அமிலங்களை அடிப்படைப் பொருளாகக் கொண்டுள்ளன. விலங்குகள் டி-ஆக்ஸிரிபோ நியூக்ளிக் அமிலத்தையும் (DNA) தாவரங்கள் ரிபோ நியூக்ளிக் அமிலத்தையும் (RNA) கொண்டுள்ளன.
காரங்கள்:
குளிப்பதற்கும், துணிகளைத் துவைப்பதற்கும் நாம் சோப்புகளைப் பயன்படுத்துகிறோம். இவை வழவழப்புத் தன்மை உடையவை. ஏன் என்று உங்களுக்குத் தெரியுமா? சோப்புகளின் வழவழப்புத் தன்மைக்குக் காரணம் அவற்றிலுள்ள காரங்கள் ஆகும். இவை தோலில் பட்டால் அரிக்கும் தன்மையையும், கசப்புச் சுவையையும் கொண்டவை. பலவகையான வெளுப்பான்கள், சோப்புகள், சலவை சோப்புகள், பற்பசைகள் மற்றும் பல பொருள்கள் காரங்களைக் கொண்டுள்ளன. அமிலங்கள் நீரில் கரைந்து ஹைட்ரஜன் அயனிகளைத் தருகின்றன. இதற்கு மாறாக, காரங்கள் நீரில் கரைந்து ஹைட்ராக்சைடு அயனிகளைத் தருகின்றன.
எனவே, நீரில் ஹைட்ராக்சைடு அயனிகளைத் தரவல்ல வேதிப்பொருள்கள் பொதுவாக காரங்கள் என அழைக்கப்படுகின்றன. எடுத்துக்காட்டு: சோடியம் ஹைட்ராக்சைடு (NaOH) மற்றும் பொட்டாசியம் ஹைட்ராக்சைடு (KOH).
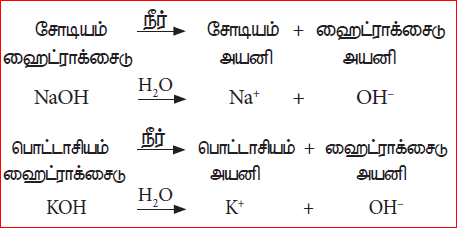
நீரில் கரையும் காரங்கள் அல்கலிகள் என்று அழைக்கப்படுகின்றன. சோடியம் ஹைட்ராக்சைடு, பொட்டாசியம் ஹைட்ராக்சைடு, கால்சியம் ஹைட்ராக்சைடு மற்றும் அம்மோனியம் ஹைட்ராக்சைடு போன்ற காரங்கள் நீரில் அதிக அளவு கரைந்து ஹைட்ராக்சைடு அயனிகளைத் தருகின்றன. எனவே, இவை அல்கலிகள் என அழைக்கப்படுகின்றன. சில வேதிச்சேர்மங்களை நீரில் கரைக்கும் பொழுது ஹைட்ராக்சைடு அயனிகளைத் தருவதில்லை. ஆனால், அவையும் காரங்களாகும். எடுத்துக்காட்டு: சோடியம் கார்பனேட், சோடியம் பைகார்பனேட், கால்சியம் கார்பனேட் போன்றவை.
சில பொதுவான காரங்கள் மற்றும் அவற்றில் காணப்படும் பொருள்கள்
| வேதிப்பெயர் | வாய்ப்பாடு | காணப்படும் பொருள்கள் |
| மெக்னீசியம்ஹைட்ராக்சைடு | Mg(OH)2 | மெக்னீசியாவின் பால்மம் |
| சோடியம் ஹைட்ராக்சைடு | NaOH | சலவை சோப்பு |
| அம்மோனியம் ஹைட்ராக்சைடு | NH4OH | ஜன்னல்களை சுத்தம் செய்வதற்குப் பயன்படும் கரைசல்கள் |
| கால்சியம் ஹைட்ராக்சைடு | Ca(OH)2 | சுண்ணாம்பு நீர் |
| பொட்டாசியம் ஹைட்ராக்சைடு | KOH | சோப்பு |
காரங்களிள் பண்புகள்:
அ. இயற்பியல் பண்புகள்:
- காரங்கள் பொதுவாக திண்ம நிலையில் காணப்படுகின்றன. ஒரு சில காரங்கள் திரவ நிலையிலும் உள்ளன. எ.கா. அம்மோனியம் ஹைட்ராக்சைடு, கால்சியம் ஹைட்ராக்சைடு.
- திரவ ஊடகத்தில் உள்ளபோது காரங்கள் வழவழப்புத் தன்மையுடன் உள்ளன.
- காரங்கள் கசப்புத் தன்மை கொண்டவை.
- காரங்கள் அரிக்கும் தன்மை கொண்டவை. இவை தோல்களின் மீது அடிக்கடி படும்போது வலிமிகுந்த கொப்பளங்களை ஏற்படுத்துகின்றன.
- காரங்கள் நிறமற்றவை.
- காரங்கள், நிறங்காட்டிகளின் நிறத்தை மாற்றுகின்றன. சிவப்பு லிட்மஸ் தாளை நீலமாகவும், மெத்தில் ஆரஞ்சு கரைசலை மஞ்சளாகவும், பினால்ப்தலீன் கரைசலை இளஞ்சிவப்பு (பிங்க்) நிறமாகவும் மாற்றுகின்றன.
- காரங்களின் நீர்க் கரைசல் மின்சாரத்தைக் கடத்துகிறது.
ஆ. வேதியியல் பண்புகள்:
- உலோகங்களுடன் வினை:
பொதுவாக காரங்கள் உலோகங்களுடன் வினைபுரிவதில்லை. அலுமினியம் மற்றும் துத்தநாகம் போன்ற உலோகங்கள் சோடியம் ஹைட்ராக்சைடுடன் வினைபுரிந்து சோடியம் அலுமினேட்டையும் ஹைட்ரஜன் வாயுவையும் தருகின்றன.
அலுமினியம் + சோடியம் ஹைட்ராக்சைடு + நீர் ???? சோடியம் அலுமினேட் + ஹைட்ரஜன்
2Al + 2NaOH + 2H2O ???? 2NaAlO2 + 3H2
- அலோக ஆக்சைடுகளுடன் வினை:
அனைத்து காரங்களும் அலோக ஆக்சைடுகளுடன் வினை புரிந்து உப்பு மற்றும் நீரைத் தருகின்றன. எடுத்துக்காட்டாக, சோடியம் ஹைட்ராக்சைடு கார்பன் டைஆக்சைடுடன் வினைபுரிந்து சோடியம் கார்பனேட்டைக் கொடுக்கிறது.
சோடியம் ஹைட்ராக்சைடு + கார்பன் டை ஆக்சைடு ???? சோடியம் கார்பனேட் + நீர்
2NaOH + CO2 ???? Na2CO3 + H2O
- அம்மோனிய உப்புகளுடன் வினை:
காரங்கள் அம்மோனிய உப்புகளுடன் வினைபுரிந்து உலோக உப்புகள், அம்மோனியா வாயு மற்றும் நீரைத் தருகின்றன.
சோடியம் ஹைட்ராக்சைடு + அம்மோனியம் குளோரைடு ???? சோடியம் குளோரைடு + அம்மோனிய வாயு + நீர்
அமிலங்களும், காரங்களும் ஒரு சில தனித்தன்மையான பண்புகளைப் பெற்றிருந்தாலும் சில பண்புகளில் அவை ஒத்துக் காணப்படுகின்றன. அவை கீழே தரப்பட்டுள்ளன.
- இவை இயற்கையில் அரிக்கும் தன்மை கொண்டவை.
- இவை நீர்க்கரைசலில் அயனியாக்கத்திற்கு உட்படுகின்றன.
- இவை நீர்க்கரைசலில் மின்சாரத்தைக் கடத்துகின்றன.
- இவை நடுநிலையாக்கல் வினைக்கு உட்படுகின்றன.
அமிலங்கள் மற்றும் காரங்களுக்கு இடையேயான வேறுபாடுகள் சில அட்டவணையில் கொடுக்கப்பட்டுள்ளன.
அமிலங்களுக்கும் காரங்களுக்கும் உள்ள வேறுபாடு
| அமிலங்கள் | காரங்கள் |
| இவை நீரில் H+ அயனிகளைத் தருகின்றன | இவை நீரில் OH- அயனிகளைத் தருகின்றன |
| இவை புளிப்புச் சுவை உடையவை | இவை கசப்புச் சுவை உடையவை |
| சில அமிலங்கள் திட நிலையில் காணப்படுகின்றன | பெரும்பாலான காரங்கள் திட நிலையில் காணப்படுகின்றன |
| அமிலங்கள் நீல லிட்மஸ் தாளை சிவப்பாக மாற்றுகின்றன | காரங்கள் சிவப்பு லிட்மஸ் தாளை நீலமாக மாற்றுகின்றன |
காரங்களின் பயன்கள்:
- குளியல் சோப்புகள் தயாரிக்க பொட்டாசியம் ஹைட்ராக்சைடு பயன்படுகிறது.
- சலவை சோப்புகள் தயாரிக்க சோடியம் ஹைட்ராக்சைடு பயன்படுகிறது.
- காகிதத் தொழிற்சாலை மற்றும் ஆடைகள் தயாரிக்கும் தொழிற்சாலைகளிலும், மருந்துகள் தயாரிக்கவும் சோடியம் ஹைட்ராக்சைடு பயன்படுகிறது.
- வெள்ளை அடிக்க கால்சியம் ஹைட்ராக்சைடு பயன்படுகிறது.
- வயிற்றில் உருவாகும் அமிலத்தன்மையை நடுநிலையாக்க அலுமினியம் ஹைட்ராக்சைடு மற்றும் மெக்னீசியம் ஹைட்ராக்சைடு போன்ற காரங்கள் பயன்படுகின்றன.
- உரங்கள், நைலான்கள், நெகிழிகள் மற்றும் இரப்பர்கள் தயாரிக்க அம்மோனியம் ஹைட்ராக்சைடு பயன்படுகின்றது.

அன்றாட வாழ்வில் காரங்களின் பயன்பாடுகள்
நடுநிலையாக்கல் வினை:
வேறுபட்ட வேதிப்பண்புகளைக் கொண்டுள்ள இரண்டு வேதிப்பொருள்கள் ஒரு வேதிவினையின் மூலம் நடுநிலை அடையும் நிகழ்வு நடுநிலையாக்கல் எனப்படும். எனவே, நடுநிலையாக்கல் என்பது அமிலமும் காரமும் வினைபுரிந்து உப்பையும் நீரையும் உருவாக்கும் வினை ஆகும். நடுநிலையாக்கல் வினையை கீழ்க்காணுமாறு குறிப்பிடலாம்.
அமிலம் + காரம் ???? உப்பு + நீர்
இந்த வினையில் ஹைட்ரோ குளோரிக் அமிலமானது H+ மற்றும் Cl– அயனிகளையும், சோடியம் ஹைட்ராக்சைடானது Na+ மற்றும் OH– அயனிகளையும் தருகின்றது. இந்த அயனிகள் இணைந்து சோடியம் குளோரைடு மற்றும் நீர் ஆகியவை உருவாகின்றன.
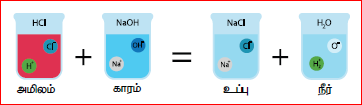
அமிலம் – காரம் வினைகள்
நடுநிலையாக்கல் வினை மூலம் உருவாகும் உப்புகள்
| அமிலம் | காரம் | உப்பு |
| ஹைட்ரோ குளோரிக் அமிலம் HCl | சோடியம் ஹைட்ராக்சைடு NaOH | சோடியம் குளோரைடு NaCl |
| சல்பியூரிக் அமிலம் H2SO4 | சோடியம் ஹைட்ராக்சைடு NaOH | சோடியம் சல்பேட் Na2SO4 |
| நைட்ரிக் அமிலம் HNO3 | சோடியம் ஹைட்ராக்சைடு NaOH | சோடியம் நைட்ரேட் NaNO3 |
| அசிட்டிக் அமிலம் CH3COOH | சோடியம் ஹைட்ராக்சைடு NaOH | சோடியம் அசிட்டேட் CH3COONa |
இதைப்போலவே, பிற அமிலங்களும் காரங்களுடன் வினைபுரிந்து உப்புகளைத் தருகின்றன. நடுநிலையாக்கல் வினை மூலம் உருவாகும் சில உப்புகள் அட்டவணையில் கொடுக்கப்பட்டுள்ளன.
நம் அன்றாட வாழ்வில் நடைபெறும் நடுநிலையாக்கல் வினைகள்:
அமிலங்களையும், காரங்களையும் சமநிலைப் படுத்துவது நமது ஆரோக்கியத்திற்கும் சுற்றுச்சூழலுக்கும் அவசியமாகும். நமது அன்றாட வாழ்வில் பல்வேறு நடுநிலையாக்கல் வினைகளைப் பார்க்கின்றோம். அவற்றுள் சில வினைகளின் முக்கியத்துவத்தைப் பற்றி இங்கு கற்போம்.
தேனீ கொட்டுதல்:
நம்மை சிவப்பு எறும்பு கடிக்கும்பொழுது அல்லது தேனீ கொட்டும்பொழுது ஃபார்மிக் அமிலமானது தோலினுள் உட்செலுத்தப்படுகிறது. இந்த அமிலமானது எரிச்சல் உணர்வினையும் வலியினையும் உண்டாக்குகிறது. வலி மற்றும் எரிச்சல் உணர்வுள்ள இடத்தில் கால்சியம் ஹைட்ராக்சைடை (வீடுகளில் பயன்படுத்தப்படும் நீற்றுச் சுண்ணாம்பு) தேய்த்து ஃபார்மிக் அமிலம் நடுநிலையாக்கப்படுகிறது.
தேனீ கொட்டுதல்
குளவி கொட்டுதல்:
குளவி கொட்டும்பொழுது, எரிச்சல் போன்ற உணர்வினையும், வலியினையும் நாம் உணர்கிறோம். இது குளவியால் நமது உடலில் செலுத்தப்படும் அல்கலி என்ற காரப்பொருளின் மூலம் ஏற்படுகிறது. இந்த காரத்தன்மையை நடுநிலையாக்க நாம் அமிலத்தன்மை கொண்ட வினிகரைப் பயன்படுத்துகிறோம்.
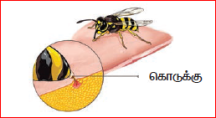
குளவி கொட்டுதல்
பற்சிதைவு:
பொதுவாக ஒரு நாளைக்கு இரண்டு முறை நாம் பல் துலக்க வேண்டும் என மருத்துவர்கள் அறிவுறுத்துகின்றனர். ஏனெனில், நம் வாயில் இருக்கும் பாக்டீரியாக்கள் பற்களுக்கு இடைப்பட்ட இடைவெளிகளில் சிக்கியுள்ள உணவுத் துகள்களைச் சிதைத்து அதன் மூலம் அமிலத்தை உருவாக்குகின்றன. இது பற்சிதைவுக்கு வழி வகுக்கிறது. இதனைத் தடுக்க நாம் அமிலத்தை நடுநிலையாக்க வேண்டும். வலிமை குறைந்த காரங்களைக் கொண்ட பற்பொடி அல்லது பற்பசையைக் கொண்டு பல் துலக்கும்போது அமிலமானது நடுநிலையாக்கப்படுகிறது. இதனால், பற்கள் வலுவாகவும், ஆரோக்கியமாகவும் இருக்கும்.
அமிலத்தன்மை:
நமது உடலில் கல்லீரல், பித்தப்பை மற்றும் கணையம் ஆகியவற்றால் சுரக்கப்படும் நொதிகளும் வயிற்றில் சுரக்கும் ஹைட்ரோகுளோரிக் அமிலமும் சேர்ந்து உணவுப் பொருள்களின் செரிமானத்திற்கு உதவுகின்றன. சில நேரங்களில் நம் வயிற்றில் சுரக்கும் ஹைட்ரோகுளோரிக் அமிலம் அதிகப்படியாக சுரப்பதால் உணவுக்குழாய் மற்றும் மார்புப் பகுதிகளில் எரிச்சல் உணர்வினை நாம் உணர்கிறோம். இது மீண்டும் மீண்டும் ஏற்பட்டால் வயிறு மற்றும் உணவுக்குழாய்களில் புண் உருவாகி, பாதிப்பு மேலும் அதிகரிக்கிறது. இதனை நடுநிலையாக்க வலிமை குறைந்த காரங்களான மெக்னீசியம் ஹைட்ராக்சைடு மற்றும் அலுமினியம் ஹைட்ராக்சைடு போன்றவற்றின் கலவை அமில நீக்கியாகப் பயன்படுகிறது. இதன் விளைவாக அமிலத்தன்மை நீக்கப்படுகிறது.
வேளாண்மை:
ஆதிக அமிலத்தன்மையுடைய மண் தாவர வளர்ச்சிக்கு ஏற்றதல்ல. எனவே, இதனைச் சரிசெய்வதற்கு விவசாயிகள் சுண்ணாம்பு (CaO), சுண்ணாம்புக் கற்கள் (CaCO3) அல்லது மரக்கட்டைகளை எரிப்பதால் கிடைக்கும் சாம்பல் ஆகியவற்றை மண்ணில் சேர்க்கின்றனர். இது மண்ணின் காரத் தன்மையை நடுநிலையாக்குகிறது.
அமில மண்
தொழில்துறை:
தொழிற்சாலைகளிலிருந்து வெளியேற்றப்படும் கழிவுகளில் சல்பியூரிக் அமிலம் உள்ளது. ஆறுகள் மற்றும் நீரோடைகளின் வழியாக கழிவுகளை வெளியேற்றும் முன் அவற்றுடன் சுண்ணாம்பு சேர்க்கப்படுகிறது. இதேபோல், மின் உற்பத்தி நிலையங்களில் மின்சாரம் தயாரிப்பதற்கு நிலக்கரி போன்ற புதைபடிவ எரிபொருள்கள் எரிக்கப்படுகின்றன. அவை எரியும்போது சல்பர் டைஆக்சைடு உருவாகிறது. எனவே, இந்த அமிலத்தன்மை மிக்க வாயு மின் நிலையங்களில் சுண்ணாம்புத்தூள் அல்லது சுண்ணாம்புக் கற்களைக் கொண்டு நடுநிலையாக்கப்படுகிறது. இவ்வாறு, சல்பர் டை ஆக்சைடால் ஏற்படும் காற்று மாசுபாடு தடுக்கப்படுகிறது.
தொழிற்சாலைக் கழிவு
நிறங்காட்டி:
நிறங்காட்டி அல்லது அமிலகார நிறங்காட்டி என்பது ஒரு வேதிப்பொருளாகும். ஒரு வேதிப்பொருள் அமிலத்தன்மை உடையதா அல்லது காரத்தன்மை உடையதா என்பதை பொருத்தமான நிறமாற்றத்தின் அடிப்படையில் இது குறிக்கிறது. இது இயற்கையானதாகவோ அல்லது செயற்கையானதாகவோ இருக்கலாம்.
இயற்கை நிறங்காட்டி:
இயற்கை நிறங்காட்டி என்பது இயற்கை மூலத்திலிருந்து பெறப்படும் வேதிப்பொருள் ஆகும். லிட்மஸ், மஞ்சள் சாறு, செம்பருத்திப் பூ மற்றும் பீட்ரூட் சாறு ஆகியவை இயற்கை மூலங்களிலிருந்து பெறப்படும் இயற்கை நிறங்காட்டிகளாகும்.
மஞ்சள் நிறங்காட்டி:
மஞ்சள் தூளில் சிறிதளவு நீரைச் சேர்த்து மஞ்சள் தூள் பசை தயாரிக்கப்படுகிறது. இது மை உறிஞ்சும் தாள் அல்லது வடிதாளின் மீது பூசப்பட்டு உலர்த்தப்படுகிறது. ஒரு கரைசலின் அமில மற்றும் காரத் தன்மையைக் கண்டறிய மஞ்சள் தூள் நிறங்காட்டி பயன்படுகிறது. அமிலக் கரைசலில் மஞ்சள் நிறங்காட்டி எந்த ஒரு குறிப்பிடத்தக்க நிற மாற்றத்தையும் தராது. அது மஞ்சளாகவே இருக்கும். ஆனால், காரக் கரைசலில் அது மஞ்சள் நிறத்திலிருந்து சிவப்பு நிறமாக மாறுகிறது.
மஞ்சள் நிறங்காட்டி
செம்பருத்திப்பூ நிறங்காட்டி:
வெந்நீரில் சில செம்பருத்திப் பூ இதழ்களைப் போட்டு 5 முதல் 10 நிமிடம் வரை ஊறவைக்கவும். இது ஒரு கரைசலை உருவாக்கும். இக்கரைசலை வடிகட்டி, நிறங்காட்டியாகப் பயன்படுத்தலாம். இந்த நிறங்காட்டியை அமிலக் கரைசலில் சேர்க்கும் போது இளஞ்சிவப்பு (பிங்க்) நிறத்தையும், காரக்கரைசலில் சேர்க்கும் போது பச்சை நிறத்தையும் அது தருகிறது.
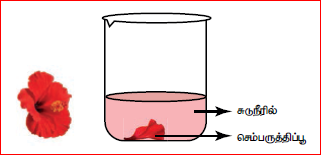
செம்பருத்தி கரைசல் நிறங்காட்டி
பீட்ருட் சாறு நிறங்காட்டி:
நாம் உண்ணும் பீட்ரூட்டிலிருந்து சாற்றை எடுத்து நிறங்காட்டியாகப் பயன்படுத்தலாம். ஒரு கரைசலானது அமிலமா அல்லது காரமா என்பதை அடையாளம் காண இது பயன்படுகிறது.
லிட்மஸ் நிறங்காட்டி:
லிட்மஸ் தாள் பொதுவாக ஆய்வகங்களில் பயன்படுத்தப்படும் ஒரு அமில-கார நிறங்காட்டி ஆகும். லிட்மஸ் என்பது ஒரு இயற்கையான நிறங்காட்டி. இது லைக்கன்களிலிருந்து பிரித்தெடுக்கப்படுகிறது. இது கரைசல் வடிவிலோ அல்லது லிட்மஸ் கரைசலை உறிஞ்சிவதன் மூலம் தயாரிக்கப்பட்ட வடிதாள் வடிவிலோ கிடைக்கின்றது. இந்தத் தாள் சிவப்பு அல்லது நீல நிறத்தில் இருக்கும். நீல லிட்மஸ் தாள் அமிலக் கரைசலில் சிவப்பு நிறமாகவும், சிவப்பு லிட்மஸ் தாள் காரக் கரைசலில் நீல நிறமாகவும் மாறும்.
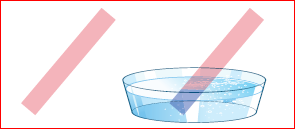
லிட்மஸ் தாள்
செயற்கை நிறங்காட்டி:
செயற்கையான பொருள்களிலிருந்து தயாரிக்கப்பட்ட நிறங்காட்டி செயற்கை நிறங்காட்டி என அழைக்கப்படுகிறது. பினாப்தலீன் மற்றும் மெத்தில் ஆரஞ்சு ஆகியவை செயற்கை நிறங்காட்டிகளுக்கு சில எடுத்துக்காட்டுகளாகும்.
பினாப்தலீன்:
பினாப்தலீன் ஒரு நிறமற்ற சேர்மம். பினாப்தலீனுடன் ஆல்கஹால் கலந்த கரைசல் நிறங்காட்டியாகப் பயன்படுகிறது. இது அமிலக் கரைசலில் நிறமற்றதாகவும், காரக் கரைசலில் இளஞ்சிவப்பு நிறமாகவும் மாறும்.
மெத்தில் ஆரஞ்சு:
சூடான நீரில் திட நிலையிலுள்ள மெத்தில் ஆரஞ்சு கரைக்கப்பட்டு வடிகட்டி நிறங்காட்டியாகப் பயன்படுத்தப்படுகிறது. இது அமிலக்கரைசலில் சிவப்பு நிறமாகவும், காரக் கரைசலில் மஞ்சளாகவும் நிறமாற்றம் அடைகிறது.
அமில மற்றும் கார ஊடகத்தில் வெவ்வேறு வகையான நிறங்காட்டிகள் அடையும் நிறமாற்றம் கீழ்க்காணும் அட்டவணையில் கொடுக்கப்பட்டுள்ளது.
நிறங்காட்டிகளின் நிறமாற்றங்கள்
| நிறங்காட்டி | அமிலக்கரைசல் | காரக்கரைசல் |
| நீல லிட்மஸ் தாள் | சிவப்பு | நிறமாற்றம் இல்லை |
| சிவப்பு லிட்மஸ் தாள் | நிறமாற்றம் இல்லை | நீலம் |
| பினாப்தலீன் | நிறமற்றது | இளஞ்சிவப்பு |
| மெத்தில் ஆரஞ்சு | சிவப்பு | மஞ்சள் |
நினைவில் கொள்க:
- அமிலங்களை நீரில் கரைக்கும் பொழுது ஹைட்ரஜன் அயனிகள் உருவாகின்றன.
- பொதுவாக அமிலங்கள் அரிக்கும் தன்மையும், புளிப்புச் சுவையும் கொண்டவை.
- நீர்த்த அமிலங்கள், உலோக ஆக்சைடுகளுடன் வினைபுரிந்து உலோக உப்புகளையும் நீரையும் தருகின்றன.
- அமிலங்கள் இரு வகைப்படும். அவை: கனிம அமிலங்கள் மற்றும் கரிம அமிலங்கள்.
- உணவுப் பொருள்கள் கெட்டுப் போகாமல் இருப்பதற்கு அசிட்டிக் அமிலம் மற்றும் பென்சாயிக் அமிலம் ஆகியவை பயன்படுத்தப்படுகின்றன.
- சல்பியூரிக் அமிலம் வேதிப் பொருள்களின் அரசன் என அழைக்கப்படுகிறது.
- காரங்கள் நீரில் கரைக்கப்படும்பொழுது ஹைட்ராக்சைடு அயனிகள் உருவாகின்றன.
- நீரில் கரையும் காரங்கள் அல்கலிகள் எனப்படும். அனைத்து அல்கலிகளும் காரங்கள். ஆனால் அனைத்துக் காரங்களும் அல்கலிகள் அல்ல.
- பொதுவாக காரங்கள் அரிக்கும் தன்மை கொண்டவை. அவை திரவத்தில் கரைந்துள்ள போது வழவழப்புடன் காணப்படுகின்றன.
- காகிதத் தொழிற்சாலைகள் மற்றும் ஆடைகள் தயாரிக்கும் தொழிற்சாலைகளிலும், மருந்து தயாரிப்பிலும் காரங்கள் பயன்படுகின்றன. உரங்கள், நைலான், நெகிழி மற்றும் இரப்பர் தயாரிப்பிலும் இவை பயன்படுகின்றன.
- அமிலமும் காரமும் வினைபுரிந்து உப்பையும் நீரையும் தருகின்ற வினை நடுநிலையாக்கல் வினை எனப்படும்.
- ஒரு குறிப்பிட்ட நிற மாற்றத்தின் மூலம் ஒரு வேதி வினையின் நிறைவைக் குறிக்கும் வேதிப்பொருள் நிறங்காட்டி எனப்படும்.
- லிட்மஸ் தாள், மஞ்சள் தூள் சாறு, செம்பருத்திப்பூ சாறு, மற்றும் பீட்ரூட் சாறு ஆகியவை இயற்கை நிறங்காட்டிகளாகும். பினால்ப்தலீன் மற்றும் மெத்தில் ஆரஞ்சு ஆகியவை செயற்கை நிறங்காட்டிகள் ஆகும்.
சொல்லடைவு:
அமிலம் – ஒன்று அல்லது அதற்கு மேற்பட்ட இடப்பெயர்ச்சி செய்யத்தக்க ஹைட்ரஜன் அணுக்களைப் பெற்றுள்ள சேர்மம்
அல்கலிகள் – நீரில் கரையும் காரங்கள்
நிறங்காட்டி – ஒரு கரைசல் அமிலத்தன்மை உள்ளதா அல்லது காரத்தன்மை உள்ளதா என்பதை பொருத்தமான நிறமாற்றத்தின் அடிப்படையில் அறியச் செய்யும் வேதிப்பொருள்
கனிம அமிலம் – தொழிற்சாலைகளில் செயற்கையாகத் தயாரிக்கப்படும் அமிலம்
இயற்கை நிறங்காட்டி – தாவரங்கிலிருந்து தயாரிக்கப்படும் நிறங்காட்டிகள்
கரிம அமிலம் – பழங்கள் மற்றும் காய்கறிகளில் இயற்கையாகக் காணப்படும் அமிலங்கள்
செயற்கை நிறங்காட்டி – மனிதர்களால் செயற்கையாகத் தயாரிக்கப்படும் நிறங்காட்டிகள்
காரம் – நீரில் கரைந்துள்ள போது ஹைட்ராக்சைடு அயனிகளைத் தரும் பொருள்
நடுநிலையாக்கல் வினை – அமிலமும் சேர்ந்து உப்பையும் நீரையும் தரும் வினை
தெரியுமா உங்களுக்கு?
ஸ்வீடன் நாட்டு வேதியியலாளர் அர்ஹீனியஸ் அமிலங்கள் பற்றிய ஒரு கொள்கையை முன் வைத்தார். அவரின் கூற்றுப்படி அமிலம் என்பது நீர்க்கரைசலில் H+ அயனிகள் அல்லது H3O+ அயனிகளைத் தரும் வேதிப்பொருளாகும்.
நமது வயிற்றில் சுரக்கும் ஹைட்ரோகுளோரிக் அமிலம் நமது வயிற்றின் உட்புறத்தை அரிப்பதால் நமக்கு பசியுணர்வு ஏற்படுகிறது. ஹைட்ரோகுளாரிக் அமிலத்தின் சுரக்கும் அளவு அதிகரித்தால் வயிற்றுப்புண் தோன்றக்கூடும்.
காப்பர் அல்லது பித்தளைப் பாத்திரங்களின் மீது வெள்ளீயம் என்ற உலோகம் (ஈயம்) பூசப்படுகிறது. அவ்வாறு பூசவில்லையெனில் உணவுப்பொருள்களிலுள்ள கரிம அமிலங்க் பாத்திரங்களிலுள்ள தாமிரத்துடன் வினைபுரிந்து உணவை நஞ்சாக்கிவிடும். வெள்ளீயம், பாத்திரங்களை அமிலங்களின் செயல்பாட்டிலிருந்து தனித்துப் பிரித்து உணவு நஞ்சாவதைத் தடுக்கின்றது.
ஊறுகாயில் வினிகர் (அசிட்டிக் அமிலம்) அல்லது பென்சாயிக் அமிலம் இருப்பதால் அவை நீண்ட நாட்கள் கெட்டுப்போகாமல் உள்ளன.
சோடியம் கார்பனேட் (Na2Co3) சலவைசோடா எனவும், சோடியம் பைகார்பனேட் (NaHCo3) சமையல் சோடா எனவும், சோடியம் ஹைட்ராக்சைடு (NaOH) காஸ்டிக் சோடா எனவும், பொட்டாசியம் ஹைட்ராக்சைடு (KOH) காஸ்டிக் பொட்டாஷ் எனவும் வணிக ரீதியாக அழைக்கப்படுகின்றன.