அணுக்கரு இயற்பியல் Notes 10th Science Lesson 6 Notes in Tamil
அணுக்கரு இயற்பியல் Notes 10th Science Lesson 6 Notes in Tamil
அறிமுகம்:
மனித இனம் அணுவைப்பற்றி தெரிந்து கொள்ள அதிக ஆர்வமும், ஈடுபாடும் கொண்டிருந்திருக்கிறது. கி.மு (பொ.ஆ.மு) 400 இல் கிரேக்கத் தத்துவ அறிஞர் டெமாகிரிட்டஸ் என்பவர் பருப்பொருள்கள் அனைத்தும் சிறிய பகுக்க இயலாத அலகுகள் எனக் கருதினார். இவை அணுக்கள் என அழைக்கப்பட்டன. அதாவது நம்மைச் சுற்றியுள்ள பொருள்கள் அனைத்தும் அணுக்களால் ஆனவை. பின்னர் 1803 இல் ஜான் டால்டன் என்பவர் தனிமங்கள் இயற்கையில் ஒரே மாதிரியான அணுக்களால் ஆனவை எனக் கருதினார். பிறகு J.J. தாம்சன் கேத்தோடு (எதிர்மின்) கதிர்கள் எனப்படும் எல்க்ட்ரான்களை ஆய்வின் மூலம் கண்டறிந்தார். அதன் பின்னர் கோல்ட்ஸ்டீன், ஆனோடு (நேர்மின்) கதிர்களை கண்டறிந்தார். பின்னாளில் அதனை புரோட்டான்கள் என ரூதர்போர்டு பெயரிட்டு அழைத்தார். மின்சுமையற்ற நியூட்ரான்களை 1932 இல் ஜேம்ஸ் சாட்விக் என்பவர் கண்டறிந்தார். தற்போது ஃபோட்டான்கள், மீசான்கள், பாசிட்ரான்கள் மற்றும் நியூட்ரினோ துகள்கள் போன்ற அடிப்படைத் துகள்கள் அதிக அளவில் கண்டறியப்பட்டுள்ளன. 1911 இல் பிரிட்டிஷ் அறிவியல் அறிஞர் எர்னஸ்ட் ருதர்போர்டு, அணுவின் நிறையானது அதன் மையத்தில் செறிந்து காணப்படுகிறது என்று விளக்கினார். இது அணுக்கரு (உட்கரு) என்றழைக்கப்படுகிறது. அணுவின் அமைப்பினைப் பற்றி நீங்கள் முந்தைய வகுப்புகளில் பயின்றுள்ளீர்கள்.
கதிரியக்கம்:
கதிரியக்கக் கண்டுபிடிப்பு:
பிரெஞ்சு இயற்பியலாளர் ஹென்றிபெக்கொரல் 1896 இல் ஆய்வுப் பணிகளை முடித்து, வாரத்தின் இறுதியில் யுரேனியம் கலந்த கூட்டுப்பொருள்களை மேசையில் விட்டுச்சென்றார். அதே மேசையில் பதிவு செய்யப்படாத ஒளிப்படத் தகட்டினையும் விட்டுச் சென்றிருந்தார். ஒரு வாரத்திற்குப் பிறகு வந்த போது மேசையிலிருந்த ஒளிப்படத்தகடு கதிரியக்கத்தால் பாதிக்கப்பட்டிருப்பதைக் கண்டறிந்தார். இதைப் போலவே யுரேனியத்திற்கு அருகில் ஒளிப்படத் தகடு வைக்கப்படும் போதெல்லாம் ஒளிப்படத்தகடு பாதிக்கப்படுவதைக் கண்டார். யுரேனியம் ஒளிப்படத்தகட்டினைப் பாதிக்கும் அளவிற்கு சில கதிர்களை வெளியிடுகிறது என்பதனை உணர்ந்தார். இந்நிகழ்வு ‘கதிரியக்கம்’ என அழைக்கப்படுகிறது. அதன் பிறகு யுரேனியம் கதிரியக்கத் தனிமமாக அடையாளப்படுத்தப்பட்டது.
இரண்டாண்டுகளுக்குப் பிறகு, போலந்து நாட்டு இயற்பியலாளர் மேரி கியூரி மற்றும் அவருடைய கணவர் பியரி கியூரியுடன் இணைந்து, பிட்ச் பிளண்ட் எனப்படும் கருமை நிற சிறிய கதிரியக்கக் கனிமத்தாதுவிலிருந்து கதிரியக்கம் வருவதைக் கண்டறிந்தனர். ஆனால் அதனை யுரேனியத்தின் தாதுவெனக் கருதியதால் இதுகுறித்து அவர்கள் வியப்படையவில்லை. இதிலிருந்து வெளியாகும் கதிர்கள் தூய்மையான யுரேனியத்திலிருந்து வரும் கதிர்களைவிட அதிக செறிவுடன் இருப்பதை அறிந்தனர். இருப்பினும் பிட்ச் பிளண்ட் எனப்படும் கதிரியக்கத் தாதுவானது யுரேனியத்தை விட குறைந்த செறிவுடையது என்பதனை உணர்ந்தனர். ஏதோ வேறு சிலப் பொருள்கள் இத்தாதுவில் இருப்பதாக முடிவு செய்தனர். அவற்றைப் பிரித்தெடுக்கும் போது அதில் தெரிந்திராத வேதிப்பண்புகள் கொண்ட புதிய பொருள் இருப்பதைக் கண்டுபிடித்தனர். யுரேனியத்தைப் போன்றே இப்புதிய பொருளும் கதிரியக்கத்தை வெளியிடுகிறது. இப்புதிய பொருளுக்கு “ரேடியம்” எனப் பெயரிட்டு அழைத்தனர். இந்தக் கதிரியக்கத் தனிமங்கள் செறிவுமிகுந்த கதிர்களான ஆல்பா, பீட்டா மற்றும் காமாக் கதிர்களை வெளிவிடுகின்றன.
கதிரியத்தின் வரையறை:
சில தனிமங்களின் உட்கருக்கள் நிலையற்றவையாக உள்ளன. இந்த உட்கருக்கள் சிதைவடைந்து சற்று அதிக நிலைப்புத்தன்மையுடைய உட்கருக்களாக மாறுகின்றன. இந்நிகழ்வே “கதிரியக்கம்” என அழைக்கப்படுகிறது. அதாவது சில தனிமங்களின் அணுக்கருக்கள் சிதைவடைந்து ஆல்பா, பீட்டா மற்றும் காமாக் கதிர்களை வெளிவிடும் நிகழ்வைக் “கதிரியக்கம்” எனவும் இந்நிகழ்விற்கு உட்படும் தனிமங்கள் அனைத்தும் “கதிரியக்கத் தனிமங்கள்” எனவும் அழைக்கப்படுகின்றன.
இயற்கைக் கதிரியக்கம்:
யுரேனியம் மற்றும் ரேடியம் போன்ற சில தனிமங்கள் கதிரியக்கத்திற்கு உட்பட்டு எவ்வித மனிதக் குறுக்கீடுகளுமின்றி கதிர்வீச்சுகளை வெளியிடுகின்றன. சில தனிமங்கள் புறத்தூண்டுதலின்றி தன்னிச்சையாக கதிர்வீச்சுகளை வெளியிடுகின்றன. இதனை இயற்கைக் கதிரியக்கம் என்று அழைக்கிறோம்.
அணு எண் 82 ஐ விட அதிகமாக உள்ள தனிமங்கள் தன்னிச்சையாக கதிரியக்கங்களை வெளியிடும் திறன் பெற்றவை. எ.கா: யுரேனியம், ரேடியம், இன்னும் பிற. அணு எண் 82 ஐ விட குறைவாக உள்ள இரண்டு தனிமங்களே இதுவரையில் கதிரியக்கத் தன்மை வாய்ந்தவை என அடையாளம் காணப்பட்டுள்ளது. அவை டெக்னிட்டியம் மற்றும் புரோமித்தியம். இந்த தனிமங்களின் அணு எண்கள் முறையே 43 மற்றும் 61 ஆகும்.
செயற்கைக் கதிரியக்கம் அல்லது தூண்டப்பட்ட கதிரியக்கம்:
செயற்கையாக அல்லது தூண்டப்பட்ட முறையில் சில இலேசான தனிமங்களை கதிரியக்கத் தனிமங்களாக மாற்றும் முறைக்கு ‘செயற்கைக் கதிரியக்கம்’என்று பெயர். இதனை மனிதர்கள் மூலம் உருவாக்கும் கதிரியக்கம் எனவும் கூறலாம்.
1934 இல் இம்மாதிரியான கதிரியக்கத்தினை ஐரின் கியூரி மற்றும் F. ஜோலியட் ஆகியோர் கண்டறிந்தனர். போரான், அலுமினியம் போன்ற சில இலேசான தனிமங்களின் உட்கருக்களை ஆல்பாத்துகளைக் கொண்டு மோதும்போது அவை தூண்டப்பட்டு செயற்கைக் கதிரியக்கத்தை வெளியிடுகின்றன. இக்கதிரியக்கத்தில் கட்புலனாகாத கதிர்வீச்சுகளும், அடிப்படைத்துகள்களும் வெளியாகின்றன. கதிரியக்கச் சிதைவின் போது, கதிரியக்கச் சிதைவிற்கு உட்படும் உட்கரு “தாய் உட்கரு” என்றும் சிதைவிற்கு பிறகு உருவாகும் உட்கரு “சேய் உட்கரு” என்றும் அழைக்கப்படுகிறது. செயற்கைக் கதிரியக்கத்தைத் தூண்டப்பயன்படும் துகள் “எறிதுகள்” அல்லது எறிபொருள் என்றும் சிதைவிற்குப் பிறகு உருவாகும் துகள் “விடுதுகள்” என்றும் பெயரிடப்பட்டுள்ளது. எறிதுகள், நிலையற்ற தாய் உட்கருவினில் மோதும்போது தன்னிச்சையாக விடுதுகளை வெளியேற்றி சேய் உட்கருவாக மாறுகிறது.
இயற்கைக் கதிரியக்கம் மற்றும் செயற்கைக் கதிரியக்கம் ஒப்பீடு
| வ.எண். | இயற்கைக் கதிரியக்கம் | சேயற்கைக் கதிரியக்கம் |
| 1 | இது அணுக்கருவின் தன்னிச்சையான சிதைவு நிகழ்வாகும் | இது அணுக்கருவின் தூண்டப்பட்ட சிதைவு நிகழ்வாகும். |
| 2 | ஆல்பா, பீட்டா மற்றும் காமாக் கதிர்கள் உமிழப்படுகின்றன | பெரும்பாலும் அடிப்படை துகள்களான நியூட்ரான், பாசிட்ரான் போன்ற துகள்கள் உமிழப்படுகின்றன. |
| 3 | இது தன்னிச்சையான நிகழ்வு | இது தூண்டப்பட்ட நிகழ்வு |
| 4 | இவை பொதுவாக 83 ஐ விட அதிக அணு எண் கொண்ட தனிமங்களில் நடைபெறுகிறது | இவை பொதுவாக 83 ஐ விட குறைவாக அணு எண் கொண்ட தனிமங்களில் நடைபெறுகிறது. |
| 5 | இதனைக் கட்டுப்படுத்த முடியாது | இதனைக் கட்டுப்படுத்த முடியும் |
X மற்றும் Y என்பது முறையே தாய் மற்றும் சேய் உட்கரு எனக் குறிப்பிடப்பட்டால், அணுக்கரு சிதைவு கீழ்க்கண்டவாறு குறிப்பிடப்படுகிறது. X (எ, வி) Y. எ மற்றும் வி என்பது எறிதுகள் மற்றும் விடுதுகள் எனக் குறிப்பிடப்படுகிறது.
எடுத்துக்காட்டாக:
4Be9 + 2He4 → 6C13*
6C13* → 6C12 + 0n1
மேற்கண்ட அணுக்கருவினையில் 6C13* என்பது நிலைப்புத் தன்மையற்றது. கதிரியக்கத் தன்மையுடையது. இவ்வினை 4Be9 (α, n) 6C12 எனக் குறிப்பிடப்படுகிறது.
4Be9 + 2He4 → 6C12 + 0n1
கதிரியக்கத்தின் அலகு:
கியூரி: இது கதிரியக்கத்தின் தொன்மையான அலகாகும். ஒரு கதிரியக்கப்பொருளிலிருந்து ஒரு வினாடியில் 3.7 x 1010 என்ற அளவில் சிதைவுகள் ஏற்பட்டால், அது ஒரு கியூரி எனப்படும். இது தோராயமாக 1 கிராம் ரேடியம் 226 ஏற்படுத்தும் சிதைவிற்குச் சமமாகும்.
1 கியூரி = ஒரு வினாடி நேரத்தில் 3.7 x 1010 சிதைவுகளைத் தரும் கதிரியக்கத் தனிமத்தின் அளவு.
ரூதர்ஃபோர்டு (Rd): இது கதிரியக்கத்தின் மற்றுமோர் அலகாகும். கதிரியக்கப் பொருளானது ஒரு வினாடியில் வெளியிடப்படும் கதிரியக்கச் சிதைவின் அளவு 106 எனில் அது ஒரு ரூதர்ஃபோர்டு என வரையறுக்கப்படுகிறது.
ஒரு ரூதர்ஃபோர்டு (Rd) = ஒரு வினாடி நேரத்தில் 106 சிதைவுகளைத் தரும் கதிரியக்கத் தனிமத்தின் அளவு.
பெக்கொரல் (Bq): கதிரியக்கத்தின் பன்னாட்டு (SI) அலகு பெக்கொரல் ஆகும். இது ஒரு வினாடியில் வெளியிடப்படும் கதிரியக்கச் சிதைவின் அளவு ஒரு பெக்கொரல் என வரையறுக்கப்படுகிறது.
ராண்ட்ஜன்: ராண்ட்ஜன் என்பது காமா (γ) மற்றும் X கதிர்களால் வெளியிடப்படும் கதிரியக்கத்தின் மற்றுமோர் அலகு. ஒரு ராண்ட்ஜன் என்பது நிலையான அழுத்தம், வெப்பநிலை மற்றும் ஈரப்பத நிலையில் 1 கிலோகிராம் காற்றில் கதிரியக்கப் பொருளானது 2.58 X 10-4 கூலும் மின்னூட்டங்களை உருவாக்கும் அளவாகும்.
ஆல்பா, பீட்டா மற்றும் காமாக் கதிர்கள்:
கதிரியக்கத்திற்கு உட்படும் கதிரியக்க உட்கரு செறிவுமிகு அல்லது அபாயகரமான கதிர்களை உமிழ்கின்றன. வழக்கமாக அவை மூன்று கதிரியக்கத் துகள்களாகத் தரப்பட்டுள்ளன. அவை ஆல்பா(α), பீட்டா (β) மற்றும் காமா (γ) கதிர்களாகும்.
ஆல்பா, பீட்டா மற்றும் காமாக் கதிர்கள் பண்புகள்:
இந்த மூன்று கதிர்களின் பண்புகளில் சில ஒற்றுமைகளும், வேற்றுமைகளும் காணப்படுகின்றன. அட்டவணையில் ஆல்பா, பீட்டா மற்றும் காமா கதிர்களின் பண்புகள் கொடுக்கப்பட்டுள்ளன.
ஆல்பா, பீட்டா, காமா கதிர்களின் பண்புகள்
| பண்புகள் | ஆல்பா (α) கதிர்கள் | பீட்டா (β) கதிர்கள் | காமா (γ) கதிர்கள் |
| தன்மை | இரண்டு புரோட்டான்கள் மற்றும் இரண்டு நியூட்ரான்கள் கொண்ட ஹீலியம் அணுவின் உட்கரு (2He4) ஆகும். | இவை அனைத்து அணுக்களிலும் காணப்படும் அடிப்படைத் துகள்களான எலக்ட்ரான்கள் ஆகும் (-1e0) . | இவை ஃபோட்டான்கள் எனப்படும் மின்காந்த அலைகளாகும். |
| மின்சுமை | இவை நேர்மின் சுமை கொண்ட துகள்கள் ஆகும். ஒவ்வொரு ஆல்பாத் துகளின் மின்சுமை = +2e | இவை எதிர்மின் சுமை கொண்ட துகள்கள் ஆகும். பீட்டாத் துகளின் மின்சுமை = -e | இவை மின்சுமையற்றவை (அ) நடுநிலைத்துகள் காமாத்துகளின் மின்சுமை = சுழி |
| அயனியாக்கும் திறன் | ஆல்பாத்துகளின் அயனியாக்கும் திறன் பீட்டாத் துகள்களை விட 100 மடங்கும், காமாத் துகள்களை விட 10,000 மடங்கும் அதிகம் | இதன் அயனியாக்கும் திறன் மிகவும் குறைவு | ஓப்பீட்டளவில் மிகவும் குறைந்த அயனியாக்கும் திறன் பெற்றவை |
| ஊடுருவும் திறன் | மிகவும் குறைந்த ஊடுருவும் திறன் உடையது. (அதாவது தடிமனான தாளைக் கொண்டு இவற்றைத் தடுத்து விட முடியும்) | ஆல்பாக் கதிர்களை விட அதிக ஊடுருவும் திறன் கொண்டவை (மெல்லிய தகட்டின் வழியே இவை ஊடுருவிச் செல்லும்) | பீட்டாக் கதிர்களை விட மிக அதிக ஊடுருவும் திறன் கொண்டவை (தடிமனான உலோகங்களின் வழியே ஊடுருவிச் செல்லும்) |
| மின் மற்றும் காந்தப் புலங்களால் ஏற்படும் விளைவு | மின் மற்றும் காந்த புலங்களால் விலக்கமடையும் (ஃப்ளமிங் இடக்கை விதிப்படி) | மின் மற்றும் காந்த புலங்களால் விலக்கமடையும். ஆனால் ஆல்பாத் துகள்கள் விலகலடையும் திசைக்கு எதிரான திசையில் விலகலடையும் (ஃப்ளமிங் இடக்கை விதிப்படி) | மின் மற்றும் காந்தப் புலங்களால் விலகலடையாது |
| திசைவேகம் | ஒளியின் திசைவேகத்தில் 1 / 10 முதல் 1 / 20 மடங்கு வரையிலான திசைவேகத்தில் செல்லும் | ஒளியின் திசைவேகத்தில் 9 / 10 மடங்கு திசைவேகத்தில் செல்லும் | ஒளியின் திசைவேகத்தில் செல்லும் |
கதிரியக்க இடம்பெயர்வு விதி:
α மற்றும் β சிதைவின் போது சேய் உட்கரு உருவாகும் என்பதனைக் கதிரியக்க இடம்பெயர்வு விதியின் மூலம் 1913 இல் சாடி மற்றும் ஃபஜன் விளக்கினர். கதிரியக்கச் சிதைவு விதி கீழ்க்கண்டவாறு கூறப்படுகிறது.
கதிரியக்கத் தனிமம் ஒன்று ஒரு α – துகளை உமிழும் போது அதன் நிறை எண்ணில் நான்கும், அணு எண்ணில் இரண்டும் என்ற அளவில் குறைந்து புதிய சேய் உட்கரு உருவாகும்.
கதிரியக்கத் தனிமம் ஒன்று β – துகளை உமிழும்போது அதன் நிறை எண்ணில் மாறாமலும், அணு எண்ணில் ஒன்று அதிகரித்தும் புதிய சேய் உட்கரு உருவாகும்.
α – சிதைவு:
அணுக்கரு வினையின் போது நிலையற்ற தாய் உட்கருவானது, α துகளை உமிழ்ந்து நிலைப்புத் தன்மையுள்ள சேய் உட்கருவாக மாறுவது α – சிதைவு என்றழைக்கப்படுகிறது.
எடுத்துக்காட்டு யுரேனியம் 238 (U238) சிதைவடைந்து, α துகளை உமிழ்ந்து, தோரியம் -234 (Th234) ஆக மாறுகிறது.
92U238 → 90Th234 + 2He4 (α – சிதைவு)
ஒரு தாய் உட்கருவானது α சிதைவடைந்து அதன் நிறை எண்ணில் நான்கும் அணு எண்ணில் இரண்டும் குறைந்து புதிய சேய் உட்கரு உருவாகும் என்பதனை விளக்குகிறது.
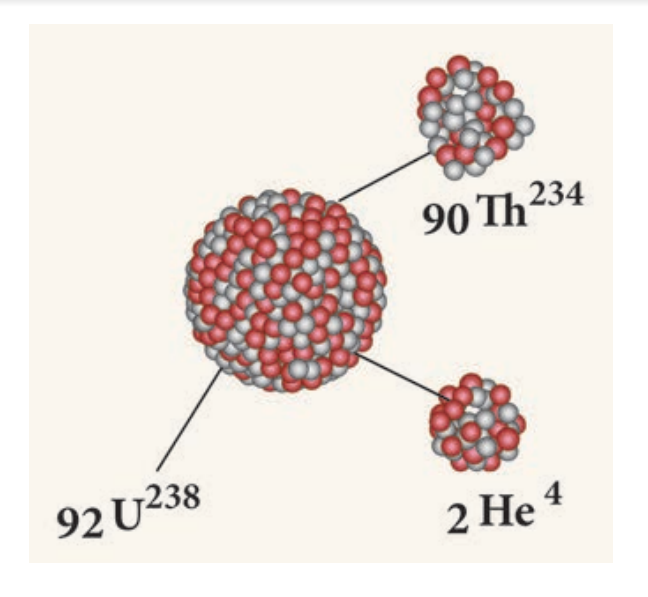
α – சிதைவு
β – சிதைவு:
அணுக்கரு வினையின் போது நிலையற்ற தாய் உட்கருவானது β துகளை உமிழ்ந்து நிலைப்புத் தன்மையுள்ள சேய் உட்கருவாக மாறுவது β – சிதைவு என்றழைக்கப்படுகிறது.
எடுத்துக்காட்டு: பாஸ்பரஸின் β – சிதைவு
15P32 → 16S32 + -1e0 ( β – சிதைவு)
β – சிதைவின் போது நிறை எண்ணில் எவ்வித மாறுபாடு இல்லாமல், அணு எண்ணில் ஒன்று அதிகரிக்கும்.
குறிப்பு: அணுக்கரு வினையில் தோன்றும் புதிய தனிமத்தின் உட்கருவானது நிறை எண்ணால் அல்லாமல் அணு எண்ணால் அறியப்படுகிறது.
γ – காமாச் சிதைவு:
காமாச் சிதைவின் போது உட்கருவின் “ஆற்றல் மட்டம்” மட்டுமே மாற்றம் அடைகிறது. அதன் அணு எண் மற்றும் நிறை எண்ணில் மாற்றம் ஏதுமில்லாமல் அதே அளவில் இருக்கும்.
அணுக்கருப்பிளவு:
வரையறை:
யுரேனியம் உட்கருவினை நியூட்ரான் கொண்டு தாக்கும் போது ஒப்பீட்டளவில் சமமான நிறைகொண்ட இரண்டு சிறு உட்கருக்களாகப் பிளவுற்று, சில நியூட்ரான்களையும் ஆற்றலையும் வெளிப்படுத்துகிறது என்பதனை 1939 இல் ஜெர்மன் அறிவியல் அறிஞர்கள் ஆட்டோஹான் மற்றும் F. ஸ்ட்ராஸ்மன் கண்டறிந்தனர்.
கனமான அணுவின் உட்கரு, பிளவுற்று இரண்டு சிறு உட்கருக்களாக மாறும் போது அதிக ஆற்றலுடன் நியூட்ரான்கள் வெளியேற்றப்படும் நிகழ்வு “அணுக்கருப் பிளவு”என்றழைக்கப்படுகிறது.
எடுத்துக்காட்டு:
யுரோனியம் 235 ( U235) இன் அணுக்கரு பிளவு
92U235 + 0n1 → 56Ba141 + 36Kr92 + 30n1 + Q (ஆற்றல்)
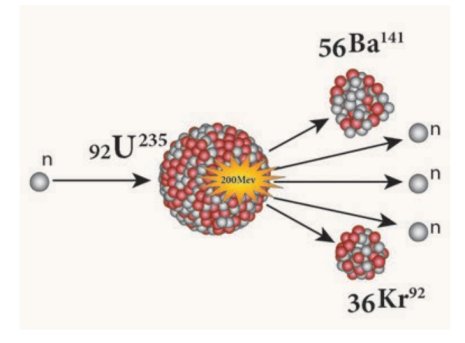
அணுக்கரு பிளவு
ஒவ்வொரு பிளவிற்கும் 3.2 x 10-11 J அளவுடைய சராசரி ஆற்றல் வெளியாகிறது. அணுக்கருப் பிளவினை விளக்குகிறது.
பிளவுக்குட்படும் பொருள்கள்:
கதிரியக்கப் பொருள் ஒன்று நியூட்ரான்களை உட்கவர்ந்து நிலைநிறுத்தப்பட்ட பிளவுகளை ஏற்படுத்துமானால் அப்பொருள் பிளவுக்குட்படும் பொருள் எனப்படும். எ.கா: யுரேனியம் 235 (U235) புளுட்டோனியம் 239 மற்றும் புளுட்டோனியம் 241 (Pu239 மற்றும் Pu241).
யுரேனியத்தின் எல்லா ஐசோடோப்புகளும், நியூட்ரான்களை உட்கவர்ந்து பிளவுக்குட்படுவதில்லை. எடுத்துக்காட்டாக, இயற்கையில் 99.28% யுரேனியம் 238 தனிமமும், மீதமுள்ள 0.72% யுரேனியம் 235 தனிமமும் கிடைக்கிறது. இவற்றில் யுரேனியம் 238 பிளவுக்குட்படுவதில்லை. அதே வேளையில் யுரேனியம் 235 பிளவுக்குட்படும் பொருளாகும்.
பிளவுக்குட்படாத சில கதிரியக்கத் தனிமங்களை நியூட்ரான்களை உட்கவரச் செய்வதன் மூலம் பிளவுக்குட்படும் பொருள்களாக மாற்றமுடியும். இவை வளமிக்க பொருள்கள் (வளமைப் பொருள்கள்) என்றழைக்கப்படுகின்றன.
எடுத்துக்காட்டு: யுரேனியம் 238, தோரியம் 232, புளுட்டோனியம் 240
தொடர்வினை:
யுரேனியம் ( U – 235) அணுக்கருவினை நியூட்ரான் கொண்டு தாக்கும் போது பிளவுக்குட்பட்டு மூன்று நியூட்ரான்கள் வெளியேற்றப்படுகின்றன. இந்த மூன்று நியூட்ரான்களும் அடுத்து வரும் மூன்று யுரேனியம் உட்கரு பிளவிற்குக் காரணமாக அமைந்து ஒன்பது நியூட்ரான்களைத் தருகின்றன. இந்த ஒன்பது நியூட்ரான்களும் மீண்டும் அடுத்த 27 நியூட்ரான்கள் உருவாக் காரணமாகின்றன. இதேபோல் இந்நிகழ்வு தொடர்ந்து நடைபெறுகிறது. எனவே இது “தொடர்வினை” என்றழைக்கப்படுகிறது. தொடர்வினையில் தன்பரவுதல் நிகழ்வின் மூலம் நியூட்ரான்களின் எண்ணிக்கை பெருக்குத் தொடர்வரிசையில் மிகவேகமாக பெருக்கமடைகின்றது.
தொடர்வினையினைக் கட்டுப்பாடான தொடர் வினை மற்றும் கட்டுப்பாடற்ற தொடர்வினை என இரண்டு வகைகளாகப் பிரிக்கலாம்.
அ. கட்டுப்பாடான தொடர்வினை:
கட்டுப்பாடான தொடர்வினையில் வெளிவரும் நியூட்ரான்களின் எண்ணிக்கை “ஒன்று” என்ற அளவில் பராமரிக்கப்படுகிறது. அதாவது, உட்கவரும் பொருட்களைக் கொண்டு வெளிவரும் நியூட்ரான்களில் ஒரே ஒரு நியூட்ரானை மட்டும் தொடர்வினைக்கு அனுமதித்து, மற்ற நியூட்ரான்கள் உட்கவரப்படுகின்றன. ஆகையால் இவ்வினையானது கட்டுப்பாடான வினையாக தொடர்கிறது. இத்தொடர்வினையின் மூலம் வெளியேற்றப்படும் ஆற்றல் ஆக்கபூர்வமான முறையில் பயன்படுத்தப்படுகின்றன. அணுக்கரு உலையில் முழுவதும் நிலைநிறுத்தப்பட்ட, கட்டுப்படுத்தப்பட்ட ஆற்றலை உருவாக்க கட்டுப்பாடான தொடர்வினையே பயன்படுத்தப்படுகிறது.
ஆ. கட்டுப்பாடற்ற தொடர்வினை:
இவ்வகை தொடர்வினையில் எண்ணற்ற நியூட்ரான்கள் பெருக்கமும், அதன் காரணமாகப் பிளவும் அதிகமான பிளவுப் பொருள்களும் உருவாகின்றன. இதன் முடிவில் ஒரு வினாடிக்குள் அதிகமான ஆற்றல் வெளியேறுகின்றது. இவ்வகை தொடர்வினையைப் பயன்படுத்தி அணு குண்டு வெடித்தல் நிகழ்த்தப்படுகிறது. இப்படம் கட்டுபாடற்ற தொடர்வினையினைக் குறிக்கிறது.
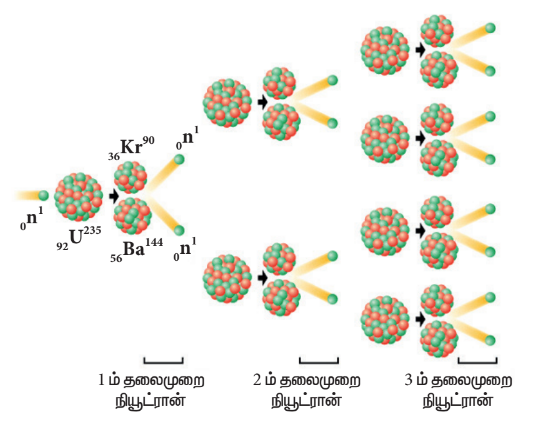
கட்டுபாடற்ற தொடர்வினை
மாறுநிலை நிறை:
அணுக்கரு பிளவின்போது 2 அல்லது 3 நியூட்ரான்கள் வெளியாகின்றன. ஆனால் எல்லா நியூட்ரான்களும் அடுத்தடுத்த பிளவினை உண்டாக்கும் என்பதனை உறுதியாகக் கூற இயலாது. சில நியூட்ரான்கள் பிளவு அமைப்பிலிருந்து வெளியேறுகின்றன. இதனை நியூட்ரான் கசிவு எனலாம். மேலும் சில நியூட்ரான்களை பிளவுக்கு உட்படாதப் பொருள்கள் உட்கவர்கின்றன.
இவ்விரு காரணிகளால் நியூட்ரான் இழப்பு ஏற்படுகிறது. தொடர்வினை நிகழ்வதற்கு அணுக்கரு பிளவு மூலம் உருவாகும் நியூட்ரான்களின் உற்பத்தி, இழப்பை விட அதிகமாக இருக்க வேண்டும். அவ்வாறு நிகழ, பிளவுக்கு உட்படும் பொருளின் நிறையானது, ஒரு குறிப்பிட்ட நிறை மதிப்பிற்குச் சமமாக இருக்க வேண்டும். இந்நிறை ‘மாறுநிலை நிறை’ எனப்படுகிறது.
தொடர்வினையைத் தொடர்ந்து நிலை நிறுத்துவதற்குத் தேவையான பிளவுப் பொருள்களின் குறைந்த அளவு நிறையை “மாறுநிலை நிறை” என அழைக்கலாம். இது அதன் சூழல், அடர்த்தி மற்றும் பிளவுக்குட்படும் பொருளின் அளவு ஆகியவற்றைச் சார்ந்தது.
மாறுநிலைநிறையை விடப் பிளவுப் பொருள்களின் நிறை குறைவாக இருந்தால் அதனை குறைமாறுநிலை நிறை (Subcritical Mass) எனலாம். மாறுநிலை நிறையை விடப் பிளவுப் பொருள்களின் நிறை அதிகமாக இருந்தால் அதனை மிகை மாறுநிலை நிறை அல்லது மீமாறுநிலை நிறை (Supercritical Mass) என அழைக்கலாம்.
அணுகுண்டு:
“கட்டுப்பாடற்ற தொடர்வினை” என்ற தத்துவத்தின் அடிப்படையில் அணு குண்டு செயல்படுகிறது. கட்டுப்பாடற்ற தொடர்வினையில் வெளிவரும் நியூட்ரான்களின் எண்ணிக்கையும், அணுக்கருப்பிளவு வினையும், பெருக்குத்தொடர் முறையில் (GP) கட்டுக்கடங்காமல் பெருகுகின்றன. மிகக் குறுகிய காலத்தில் அதிக ஆற்றலுடன் கூடிய பெரு வெடிப்பு நிகழ்கிறது.
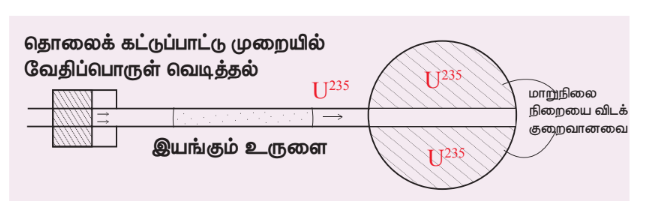
அணு குண்டு
அமைப்பு:
அணுகுண்டில் குறைமாறுநிலை நிறை கொண்ட பிளவுக்கு உட்படும் பொருளின் ஒரு சிறுபகுதி வைக்கப்பட்டுள்ளது. இந்த சிறுபகுதியானது உருளை வடிவ வெற்றிடத்தைக் கொண்டுள்ளது. வெற்றிடத்திற்குப் பொருந்தும் வகையில், உருளை வடிவப் பிளவுக்குட்படும் பொருள் ஒன்று வைக்கப்படுகிறது. இதன் நிறை, மாறுநிலை நிறையைவிடக் குறைவாக இருக்க வேண்டும். அணு குண்டு வெடிப்பிற்காக இந்த உருளையானது வெற்றிடத்திற்குள்ளே ஊடுருவச் செய்யப்படுகிறது. இவ்விரு பகுதிகளும் ஒன்றாகச் சேர்ந்து மீமாறுநிலை நிறையை (supercritical mass) அடைந்தவுடன் அணுகுண்டு வெடிப்பு நிகழ்கிறது.
அணுகுண்டு வெடிப்பு நிகழ்வின் போது மிக அதிக அளவு ஆற்றலுடன் வெப்பமும் ஒளியும், கதிரியக்கமும் வெளியாகின்றன. மிகக்குறுகிய வினாடிகளுக்குள் கட்டுக்கடங்காத அழுத்தமும், வெப்பமும் மிக அதிக அளவில் உயர்கிறது. அனைத்து உயிரினங்களுக்கும் தீங்கிழைக்கக் கூடிய காமாக் கதிர்வீச்சுகள் இத்துடன் வெளியாகின்றன. 1945 இல் இரண்டாம் உலகப்போரின்போது ஜப்பானில் உள்ள ஹிரோஷிமா மற்றும் நாகசாகி பகுதிகளில் இவ்வகையான அணுகுண்டுகள் வீசப்பட்டன.
அணுக்கரு இணைவு:
கனமான அணுக்கரு பிளவுற்று இரண்டு சிறிய அணுக்கருகளாக பிளவுறும் போது ஆற்றல் வெளியாகிறது என்பதனைப் பயின்றுள்ளீர்கள் அல்லவா?. இதனைப் போன்றே இரு இலேசான உட்கருக்கள் இணைந்து கனமான உட்கரு உருவாகும் போதும் ஆற்றல் வெளியாகிறது. இந்த நிகழ்வினை “அணுக்கரு இணைவு” எனலாம்.வரையறை:
மிக இலேசான இரு அணு உட்கருக்கள் இணைந்து கனமான அணுக் கருவினை உருவாக்கும் நிகழ்வு “அணுக்கரு இணைவு”எனலாம்.
எடுத்துக்காட்டு:
1H2 + 1H2 → 2He4 + Q (ஆற்றல்)
1H2 என்பது ஹைட்ரஜனின் ஐசோடோப்பான டியூட்ரியத்தைக் குறிக்கிறது. ஒவ்வொரு அணுக்கரு இணைவின் போதும் வெளியாகும் சராசரி ஆற்றல் 3.814 x 10-12 J. இதனைப் படம் குறிக்கின்றது.
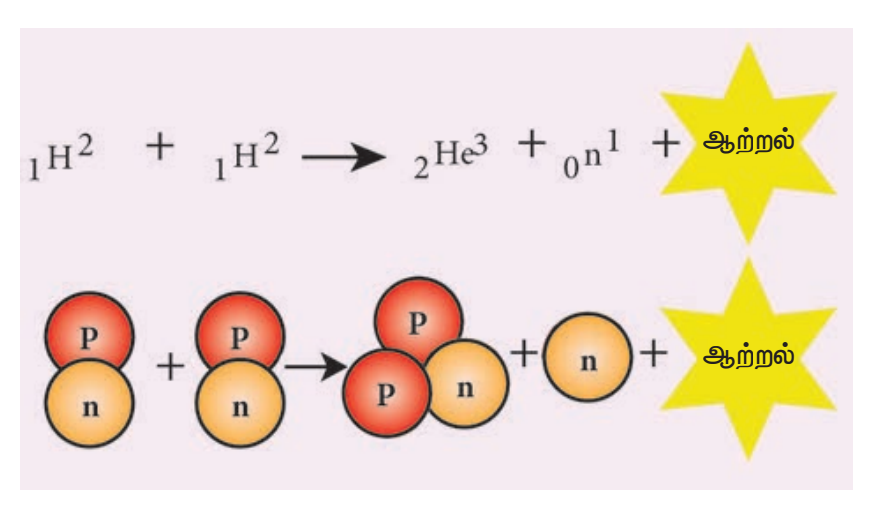
அணுக்கரு இணைவு
அணுக்கருவினையின் போது (இணைவு மற்றும் பிளவு) உருவாகும் சேய் உட்கருவின் நிறையானது இரண்டு தாய் உட்கருக்களின் நிறைகளின் கூடுதலை விடக் குறைவாக இருக்கும். தாய் உட்கருவின் நிறைக்கும், சேய் உட்கருவின் நிறைக்கும் இடையே உள்ள நிறைவேறுபாடு “நிறைவழு” என அழைக்கப்படுகிறது. இந்த நிறைவேறுபடானது ஆற்றலாக (நிறை ஆற்றல் சமன்பாடு) மாற்றமடைகிறது. இந்தக்கருத்தினை 1905 இல், நிறை ஆற்றல் சமன்பாடு மூலமாக ஐன்ஸ்டீன் முன்மொழிந்தார். அதாவது நிறை ஆற்றலாகவும், ஆற்றல் நிறையாகவும் மாறும் என்பதனை நிறை ஆற்றல் சமன்பாடு வலியுறுத்துகிறது. நிறை ஆற்றல் சமன்பாட்டிற்கான தொடர்பு E = mc2. இதில் c என்பது ஒளியின் திசைவேகம் ஆகும். வெற்றிடத்தில் இதன் மதிப்பு 3 x 108 மீவி-1.
அணுக்கரு இணைவிற்கான நிபந்தனைகள்:
பூமியைச் சுற்றியுள்ள வளிமண்டலத்தில் மிகக் குறைந்த அளவு ஹைட்ரஜன் உள்ளது. சாதாரண வெப்பம் மற்றும் அழுத்தத்தில் அணுக்கரு இணைவு நடைபெற்றால் வளிமண்டலத்தில் ஹைட்ரஜன் வெடிப்பு நிகழ்ந்திருக்கக்கூடும் அல்லவா? ஆனால் அதுபோன்று நிகழவில்லையே ஏன்? என்பதனை உங்களால் விளக்கமுடியுமா?
அணுக்கரு இணைவானது கீழ்க்கண்ட நிபந்தனைக்குட்பட்டே நிகழக்கூடும் என்பதே இதற்கான விடை ஆகும்.
107 முதல் 109 K என்ற மிக உயர்ந்த வெப்பநிலையிலும், உயர் அழுத்தத்திலும் மட்டுமே அணுக்கரு இணைவு நடைபெறும். அதாவது இந்நிலையில் ஹைட்ரஜன் அணுவின் உட்கருக்கள் ஒன்றோடு ஒன்று அருகருகே சென்று அணுக்கரு இணைவு நடைபெறும். அதனால் இதனை “வெப்ப அணுக்கரு இணைவு”என்றழைக்கின்றோம்.
விண்மீன் ஆற்றல்:
சூரியனைப் போன்ற விண்மீன்கள், அதிக அளவு ஆற்றலை ஒளி மற்றும் வெப்ப வடிவில் உமிழ்கின்றன. இந்த ஆற்றலானது விண்மீன் ஆற்றல் எனப்படும். அதிக அளவு ஆற்றலானது எங்கிருந்து வெளியாகிறது?
அனைத்து விண்மீன்களும் அதிக அளவில் ஹைட்ரஜனை தன்னகத்தேக் கொண்டுள்ளன. விண்மீன்களின் புறப்பரப்பு வெப்பநிலை மிக அதிகம். இந்த வெப்பநிலை ஹைட்ரஜனின் அணுக்கரு இணைவிற்கு போதுமானதாக இருக்கும். மேலும் சூரியன் மற்றும் விண்மீன்களின் உள் அடுக்கில் அணுக்கரு இணைவு நடைபெறுவதால் அதிக அளவு ஆற்றல் உருவாகிறது. இது “விண்மீன் ஆற்றல்” எனப்படும். இதனை “அணுக்கரு இணைவு” அல்லது “வெப்ப அணுக்கரு வினை” எனவும் அழைக்கலாம். இதுவே சூரியன் மற்றும் விண்மீன்களின் ஒளி மற்றும் வெப்ப ஆற்றலுக்கான மூலமாக இருக்கிறது.
ஹைட்ரஜன் குண்டு:
அணுக்கரு இணைவு தத்துவத்தின் அடிப்படையில் ஹைட்ரஜன் குண்டு செயல்படுகிறது. இதற்குத் தேவையான உயர் வெப்பநிலையையும், அழுத்தத்தையும் உருவாக்க, அணு குண்டு ஒன்று வெடிக்கச் செய்யப்படுகிறது. இதன் பிறகு, ஹைட்ரஜனில் அணுக்கரு இணைவானது நடைபெற்று, கட்டுக்கடங்காத அளவு அதிக ஆற்றல் வெளியாகிறது. ஹைட்ரஜன் குண்டின் மூலம் (அணுக்கரு இணைவு) உருவாகும் ஆற்றலானது, அணுகுண்டின் மூலம் (அணுக்கரு பிளவு) உருவாகும் ஆற்றலை விட அதிகமாகும்.
அணுக்கரு பிளவு மற்றும் அணுக்கரு இணைவின் தன்மைகள்
| அணுக்கரு பிளவு | அணுக்கரு இணைவு |
| கனமான அணுக்கருக்கள் பிளவுற்று இலேசான அணுக்கருக்களாக மாறும் நிகழ்வு “அணுக்கரு பிளவு” என்றழைக்கப்படுகிறது. | இரண்டு இலேசான அணுக்கருக்கள் இணைந்து கனமான அணுக்கருக்களாக மாறும் நிகழ்வு அணுக்கரு இணைவு எனப்படும். |
| அறை வெப்பநிலையிலும் இந்நிகழ்வு நிகழக்கூடும். | அணுக்கரு இணைவிற்கு உயர் வெப்பநிலை மற்றும் அழுத்தம் தேவை. |
| ஆல்பா, பீட்டா மற்றும் காமாக் கதிர்கள் வெளியாகின்றன. | ஆல்பாக் கதிர்கள், பாசிட்ரான்கள் மற்றும் நியூட்டிரினோக்கள் வெளியாகின்றன. |
| அணுக்கரு பிளவு காமாக் கதிர்களை வெளியிடுவதால் இவை மனித ஜீன்களைத் தூண்டி மரபியல் மாற்றத்தை உண்டாக்கி பரம்பரை நோய்களுக்குக் காரணமாக அமைகிறது. | வெப்பமும் ஒளியும், உமிழப்படுகின்றன. |
கதிரியக்கத்தின் பயன்கள்:
கதிரியக்கத்தின் மூலமாகப் பல்வேறு கதிரியக்க ஐசோடோப்புகளைப் பெற இயலும். மருத்துவம், வேளாண்மை தொழிற்சாலை மற்றும் தொல்லியல் ஆய்வு போன்ற பல்வேறு துறைகளில் கதிரியக்க ஐசோடோப்பு பயன்படுகின்றன.
வேளாண்மை:
கதிரியக்கப் பாஸ்பரஸ் ஐசோடோப் P – 32 பயிர் உற்பத்தியை அதிகரிக்கப்பயன்படுகிறது. பூச்சிகள் மற்றும் ஒட்டுண்ணிகள் போன்ற நுண்ணுயிரிகளால் வேளாண் உற்பத்திப்பொருள்கள் கெட்டுப்போகாமல் நுண்ணுயிரிகளை அழித்து, வேளாண் உற்பத்திப் பொருள்களைப் பாதுகாக்கவும் கதிரியக்க ஐசோடோப்புகள் பயன்படுகின்றன. சேமிக்கப்படும் சிலவகை தானியங்களை கதிரியக்கத்திற்கு உட்படுத்தி, அவைகளை நீண்ட நாள்களுக்கு அதே புதுத்தன்மையோடு பயன்படுத்திட இயலும். சிறிதளவு கதிர்வீச்சின் மூலம் வெங்காயம், உருளைக்கிழங்கு ஆகியவற்றை அழுகிப் போகாமல் இருக்கச் செய்யவும், பருப்பு வகைத் தானியங்களைச் சேமிப்புக் காலத்தில் முளைவிடாமல் பாதுகாக்கவும் இயலும்.
மருத்துவம்:
கதிரியக்க ஐசோடோப்புகள் மருத்துவத்துறையில் இரண்டு வகைகளில் வகைப்படுத்தப்பட்டு பயன்படுத்தப்படுகிறது.
- நோயறிதல்
- கதிரியக்க சிகிச்சை
ரத்தச் சுழற்சியில் உள்ள குறைபாடுகளை அறியவும், எலும்புகளில் வளர்சிதை மாற்றக் குறைபாட்டினை அறியவும், மூளையில் உள்ள கட்டிகளை அறியவும் கதிரியக்க ஐசோடோப்புகள் பயன்படுகின்றன. ஹைட்ரஜன், கார்பன், நைட்ரஜன் சல்பர் போன்ற சில கதிரியக்க ஐசோடோப்புகள் நோய்களைக் கண்டறியப் பயன்படுகின்றன.
- கதிரியக்கச் சோடியம் – 24 (Na24) இதயத்தை சீராகச் செயல்பட வைக்க உதவுகிறது.
- கதிரியக்க அயோடின் – 131 (I131) முன் கழுத்துக் கழலையைக் குணப்படுத்த உதவுகிறது.
- இரும்பின் ஐசோடோப்பான இரும்பு – 59 (Fe59) ரத்தச் சோகையை அடையாளம் காணவும் குணப்படுத்தவும் உதவுகிறது.
- கதிரியக்கப் பாஸ்பரஸ் – 32 (P32) தோல் நோய்ச் சிகிச்சையில் பயன்படுகிறது.
- கதிரியக்கக் கோபால்ட் – 60 (Co60) மற்றும் தங்கத்தின் ஐசோடோப்பான தங்கம் – 198 (Au198) தோல்புற்று நோயைக் குணப்படுத்தப்பயன்படுகிறது.
- அறுவைச்சிகிச்சைக்குப் பயன்படும் சாதனங்களில் காணப்படும் நுண்கிருமிகளைக் கதிரியக்கத்தின் மூலம் நீக்கி தூய்மை செய்யப்படுகிறது.
தொழிற்சாலை:
தொழிற்சாலைகளில் தயாரிப்பின்போது ஏற்படும் உற்பத்திக் குறைபாடுகளான விரிசல்கள் மற்றும் கசிவுகளைக் கண்டறிய கதிரியக்க ஐசோடோப்புகள் பயன்படுகின்றன. பல்வேறு தொழிற்சாலைகளில் வாயுக்கள், திரவங்கள் மற்றும் திண்மங்களின் அளவுகளைக் கண்டறிய கதிரியக்க மூலங்கள் பயன்படுகின்றன.
- வானூர்திகளில் எடுத்துச் செல்லப்படும் சுமைகளில் வெடி பொருள்கள் உள்ளனவா? என்பதனைக் கண்டறிய கலிபோர்னியம் – 252 (Cf252) பயன்படுகிறது.
- பல்வேறு தொழிற்சாலைகளில் புகையை உணரும் கண்டுணர்வியாக அமர்சியம் – 241 (Am241) ஐசோடோப்புகள் பயன்படுகின்றன.
தொல்லியல் ஆய்வு:
கதிரியக்கக் கார்பன் வயது கணிப்பு நுட்பத்தைப் பயன்படுத்தி பூமியின் வயது, படிமப் பொருள்கள், பழமையான ஓவியங்கள் மற்றும் நினைவிடங்கள் ஆகியவற்றின் வயதினை அறியப் பயன்படுகிறது. அதாவது கார்பன் வயது கணிப்பு மூலம் பொருள்களில் பொதிந்துள்ள கதிரியக்கக் கார்பனின் அளவைக் கொண்டு அவற்றின் வயதினைக் கணிக்கலாம்.
பாதுகாப்பு வழிமுறைகள்:
அன்றாடம் நீங்கள் சூரியனிடமிருந்து சில இயற்கைக் கதிரியக்கங்களைப் பெறுகின்றீர்கள். மேலும் மண் மற்றும் பாறைகள், வீட்டு உபயோகப் பொருள்களான தொலைக்காட்சி, நுண்ணலைச் சூடேற்றி (micro oven), அலை பேசி மற்றும் மருத்துவ துறையில் பயன்படும் x கதிர்கள் ஆகியவற்றிலிருந்து கதிரியக்கங்கள் வெளியாகின்றன. இவை மிகக் குறைந்த செறிவைப் பெற்றுள்ளதால் கடுமையான பாதிப்புகளை ஏற்படுத்துவதில்லை.
அணுக்கரு சோதனைகளை வளிமண்டலத்திலும், பூமிக்கடியிலும் நிகழ்த்துவதால் வெளியாகும் கதிர்வீச்சுகளும், அணுக்கரு உலையிலிருந்து வெளியாகும் கதிர்வீச்சுகளுமே மனிதன் உருவாக்கிய இரண்டாவது கதிரியக்க மூலமாகக் கருதப்படுகிறது.
கவனக் குறைவாகவும் முறையின்றியும் கதிரியக்கப் பொருள்களை கையாள்வதால், மனிதர்களுக்குத் தீங்கினை ஏற்படுத்தக்கூடிய அபாயகரமானக் கதிர்வீச்சுகள் வெளியாகின்றன. மேலும் நீண்ட காலம் கதிரியக்கங்களுக்கு மிக அருகில் பணி செய்யும் ஒருவரின் உடல்நலம் மிகுந்த பாதிப்புக்குள்ளாவதுடன் மரபியல் ரீதியாகவும் பாதிக்கப் படக்கூடும்.
அனுமதிக்கப்பட்ட அளவு:
மனித உடலின்மீது கதிர்வீச்சுப் படும்போது பாதிப்பை ஏற்படுத்தாத கதிர்வீச்சின் பெரும அளவை பன்னாட்டு கதிரியக்கப் பாதுகாப்புக் கழகம் (ICRP) பரிந்துரை செய்துள்ளது. ஓர் ஆண்டிற்கான கதிரியக்கப் பாதிப்பின் பாதுகாப்பான அளவு 20 மில்லி சிவர்ட் ஆகும். இதனை ராண்ட்ஜன் அலகில் குறிப்பிடும்போது கதிர்வீச்சு ஒரு வாரத்திற்கு 100 மில்லி ராண்டஜன் என்ற அளவில் இருக்க வேண்டும். கதிர்வீச்சுப் பாதிப்பு 100 R என்றிருந்தால் மிகவும் அபாயகரமான பாதிப்பான ரத்தப் புற்று நோயை (ரத்தச் சிவப்பணுக்களின் அழிவு) ஏற்படுத்தும், கதிர்வீச்சுப் பாதிப்பு 600 R என்ற அளவில் இருக்கும்போது இறப்பை உண்டாகும்.
தடுப்பு வழிமுறைகள்:
கதிரியக்கப் பொருள்களைத் தடிமனான காரீயச் சுவர்களால் ஆன கொள்கலனில் வைக்க வேண்டும்.

காரீயத்திலான மேலாடை (மாதிரி)
- அபாயகரமான கதிரியக்கப்பகுதிகளில் பணிபுரிவோர் காரீய கையுறைகளையும் காரீயத்தினாலான மேலாடையையும் கட்டாயமாக அணிய வேண்டும்.
- கதிரியக்கப் பொருள்களைக் கையாளும் போது உணவருந்துவதை தவிர்க்க வேண்டும்.
- கதிரியக்கப் பொருள்களை இடுக்கிகள் அல்லது தொலைக்கட்டுப்பாட்டு கருவி (remote) ஆகியவற்றை பயன்படுத்தி மட்டுமே கையாள வேண்டும். நேரடியாக தொட்டுப் பயன்படுத்தக்கூடாது.
- டோசிமீட்டரை அணிந்து கொள்வதன் மூலம் கதிரியக்கத்தினைப் பயன்படுத்துவோர் எடுத்துக் கொள்ளும் கதிரியக்க அளவினை அவ்வப்போது அறிந்து கொள்ள இயலும்.
அணுக்கரு உலை:
அணுக்கரு உலை என்பது முழுவதும் தற்சார்புடைய கட்டுப்படுத்தப்பட்ட அணுக்கரு பிளவு வினை நடைபெற்று மின் உற்பத்திச் செய்யும் இடமாகும். 1942 இல் அமெரிக்காவில் உள்ள சிகாகோ நகரில் முதல் அணுக்கரு உலை கட்டப்பட்டது.
அணுக்கரு உலையின் வகைகள்:
உற்பத்தி உலை, வேக உற்பத்தி உலை, அழுத்த நீர்ம உலை, கன அழுத்த நீர்ம உலை, கொதி நீர் உலை, குளிரூட்டப்பட்ட நீர்ம உலை, குளிரூட்டப்பட்ட வாயு உலை, அணுக்கரு இணைவு உலை மற்றும் வெப்ப அணுக்கரு உலை ஆகியவை உலக் அளவில் பயன்பாட்டில் உள்ள சில அணுக்கரு உலைகளாகும்.
அணுக்கரு உலையின் பகுதிக் கூறுகள் (அ) முதன்மையான பாகங்கள்:
அணுக்கரு உலையின் இன்றியமையாத பாகங்கள்
- எரிபொருள்
- தணிப்பான்கள்
- கட்டுப்படுத்தும் கழிகள்
- குளிர்விப்பான் மற்றும்
- தடுப்புச்சுவர்
- எரிபொருள்: பிளவுக்குட்படும் பொருளே எரிபொருளாகும், அணுக்கரு உலையில் பொதுவாகப் பயன்படும் எரிபொருள் யுரேனியம் ஆகும்.
- தணிப்பான்: உயர் ஆற்றல் கொண்ட நியூட்ரான்களைக் குறைந்த ஆற்றல் கொண்ட நியூட்ரான்களாகக் குறைப்பதற்குத் தணிப்பான் பயன்படுகிறது. கிராஃபைட் மற்றும் கனநீர் ஆகியவை பொதுவாகப் பயன்படும் தணிப்பான்களாகும்.
- கட்டுப்படுத்தும் கழி: தொடர்வினையை நிலை நிறுத்தி நியூட்ரான்களின் எண்ணிக்கையைக் கட்டுப்படுத்துவதற்காகப் பயன்படுவது கட்டுப்படுத்தும் கழியாகும். போரான் மற்றும் காட்மியம் கழிகளே பெரும்பாலும் கட்டுப்படுத்தும் கழிகளாகப் பயன்படுத்தப்படுகின்றன. இவை நியூட்ரான்களை உட்கவரும் திறன் பெற்றவை.
- குளிர்விப்பான்: அணுக்கரு உலையினுள் உருவாகும் வெப்பத்தை நீக்குவதற்காகக் குளிர்விப்பான் பயன்படுகிறது. இதில் உருவாகும் நீராவியைக் கொண்டு விசையாழியை இயக்கி மின் உற்பத்தி செய்யப் பயன்படுகிறது. நீர், காற்று மற்றும் ஹீலியம் ஆகியவை சில குளிவிப்பான்களாகும்.
- தடுப்புச்சுவர்: அபாயகரமான கதிர்வீச்சு சுற்றுப்புறச் சூழலில் பரவாமல் தடுத்து பாதுகாப்பதற்காகத் தடிமனான காரீயத்தலான சுவர் அணுக்கரு உலையைச் சுற்றி கட்டப்படுகிறது.
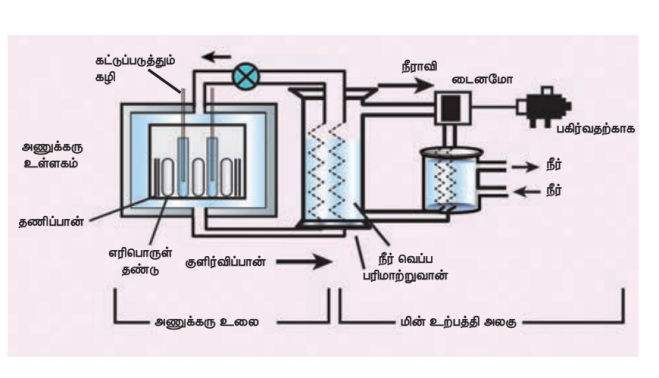
அணுக்கரு உலை
அணுக்கரு உலையின் பயன்கள்:
அணுக்கரு உலையானது அதிக அளவில் மின் உற்பத்திக்காகப் பயன்படுகிறது.
பல விதமான பயன்பாடுகளை உடைய கதிரியக்க ஐசோடோப்புகளை உருவாக்கப் பயன்படுகிறது.
அணுக்கரு இயற்பியல் துறையில் ஆய்வினை மேற்கொள்வதற்காகச் சில அணுக்கரு உலைகள் பயன்படுகின்றன.
பிளவுக்கு உட்படாத பொருட்களைப் பிளவுக்கு உட்படும் பொருள்களாக மாற்றுவதற்கு உற்பத்தி உலைகள் பயன்படுகின்றன.
இந்திய அணுமின் நிலையங்கள்:
1948 ஆம் ஆண்டு ஆகஸ்டு மாதத்தில் இந்திய அறிவியல் ஆராய்ச்சித் துறையால் இந்திய அணுசக்தி ஆணையம் (AEC) மும்பையில் அமைக்கப்பட்டது. இதன் தலைவராக டாக்டர் ஹோமி ஜஹாங்கிர் பாபா முதன்முதலில் பொறுப்பு வகித்துள்ளார். அணுசக்தி துறையில் நடைபெறும் அனைத்து ஆய்வுகளும் இந்த நிறுவனத்தின் மூலமே மேற்கொள்ளப்படுகிறது. இது தற்போது பாபா அணு ஆராய்ச்சி மையம் (BARC) என அழைக்கப்படுகிறது.
இந்திய மின் உற்பத்தியில், அணு சக்தியானது ஐந்தாவது வளமாக உள்ளது. தாராப்பூர் அணுமின்நிலையம் இந்தியாவின் முதல் அணுமின்நிலையமாகும். மகாராஷ்டிரா, ராஜஸ்தான், குஜராத், உத்திரப்பிரதேசம், கர்நாடகா ஆகிய மாநிலங்களில் தலா ஒரு அணுமின்நிலையமும் தமிழ்நாட்டில் இரண்டு அணுமின் நிலையங்கள் என ஏழு அணுமின்நிலையங்கள் உள்ளன. தமிழ்நாட்டில் கல்பாக்கம் மற்றும் கூடங்குளம் ஆகிய இரண்டு இடங்களில் அணுமின்நிலையங்கள் அமைந்துள்ளன. ஆசியா மற்றும் இந்தியாவில் கட்டப்பட்ட முதல் அணுக்கரு உலை அப்சரா ஆகும். இந்தியாவில் தற்போது 22 அணுக்கரு உலைகள் செயல்பாட்டில் உள்ளன. மற்ற சில செயல்படும் அணுக்கரு உலைகள்:
- சைரஸ்
- துருவா
- பூர்ணிமா
தீர்க்கப்பட்ட கணக்கு:
1. கீழ்க்கண்ட அணுக்கரு வினையிலிருந்து A, B, C மற்றும் D ஆகியவற்றைக் காண்க,
- 13Al27 + A ——–> 15P30 + B
- 12Mg24 + B ——-> 11Na24 + C
- 92U238 + B ——–> 93Np239 + D
தீர்வு:
- 13Al27 + 2He4 ———-> 15P30 + 0n1
- 12Mg24 + 0n1 ———–> 11Na24 + 1H1
- 92U238 + 0n1 ————> 93Np239 + -1e0
A என்பது ஆல்பாத் துகள், B என்பது நியூட்ரான், C என்பது புரோட்டான் மற்றும் D என்பது எலக்ட்ரான்.
தீர்க்கப்பட்ட கணக்கு:
2. ஒரு ராடான் மாதிரியிலிருந்து ஒரு வினாடியில் 3.7 x 103 GBq கதிரியக்கம் வெளியாகிறது எனில் இச்சிதைவினை கியூரி அலகாக மாற்றுக.
ஒரு கியூரி = 3.7 x 1010 Bq (ஒரு வினாடியில் ஏற்படும் சிதைவு)
தீர்வு:
1 Bq = ஒரு வினாடியில் ஏற்படும் சிதைவு
ஒரு கியூரி = 3.7 x 1010 Bq
1 Bq = 1 / 3.7 x 1010 கியூரி
3.7 x 103 G Bq = 3.7 x 103 x 109 x 1 / 3.7 x 1010
= 100 கியூரி
தீர்க்கப்பட்ட கணக்கு:
3. 92U235 ஒரு ஆல்பா சிதைவிற்கும் ஒரு பீட்டா சிதைவிற்கும் உட்படுகிறது. இறுதியில் புதிதாகத் தோன்றும் உட்கருவில் உள்ள நியூட்ரான்களின் எண்ணிக்கையைக் காண்க.
தீர்வு:
X மற்றும் Y என்பன ஆல்பா மற்றும் பீட்டா துகள் உமிழ்விற்குப் பிறகு முறையே உருவாகும் புதிய தனிமங்களாகும்.
92U235 α சிதைவு 90X231 + 2He4
→
90X231 β சிதைவு 91Y231 + -1e0
→
நியூட்ரான்களின் எண்ணிக்கை = நிறை எண் – அணு எண்
= 231 – 91 = 140
தீர்க்கப்பட்ட கணக்கு:
2 கிகி நிறையுடைய ஒரு கதிரியக்கப் பொருளானது அணுக்கரு இணைவின்போது வெளியாகும் மொத்த ஆற்றலைக் கணக்கிடுக.
தீர்வு:
வினையின் போது நிறைவழு m = 2கிகி
ஒளியின் திசைவேகம் c = 3 x 108 மீவி-1
ஐன்ஸ்டீன் நிறை ஆற்றல் சமன்பாடு E = mc2
E = 2 x ( 3 x 108)2
= 1.8 x 1017 J
நினைவில் கொள்க:
- புறத்தூண்டுதலின்றி தன்னிச்சையாக நடைபெறும் கதிரியக்க உமிழ்வு இயற்கைக் கதிரியக்கம் என்றழைக்கப்படுகிறது.
- கதிரியக்கப் பொருளானது ஒரு வினாடியில் வெளியிடப்படும் கதிரியக்கத்தின் அளவு 3.7 x 1010 எனில் அது ஒரு கியூரி எனப்படும். ஒரு கியூரி = 3.7 x 1010 ஒரு வினாடியில் நிகழும் சிதைவு.
- ரூதர்ஃபோர்டு Rd : கதிரியக்கப் பொருளானது ஒரு வினாடியில் வெளியிடப்படும் கதிரியக்கச் சிதைவின் அளவு 106 எனில் அது ஒரு ரூதர்ஃபோர்டு என வரையறுக்கப்படுகிறது.
- கதிரியகத்தின் பன்னாட்டு அலகு 1 பெக்கொரல். ஒரு வினாடியில் வெளியிடப்படும் கதிரியக்கச் சிதைவின் அளவு ஒரு பெக்கொரல் என வரையறுக்கப்படுகிறது.
- ஹீலியம் உட்கரு (2He4) என்பது இரண்டு புரோட்டான்கள் மற்றும் இரண்டு நியூட்ரான்களைக் கொண்ட ஆல்பாத் துகள் ஆகும்.
- பீட்டா துகள்கள் என்பன எல்லா அணுக்களிலும் அமைந்துள்ள அடிப்படைத்துகள்களான எலக்ட்ரான்கள் (-1e0) ஆகும்.
- நிலைப்புத் தன்மையற்ற தாய் உட்கருவிலிருந்து ஆல்பாத் துகளை உமிழ்ந்து நிலைப்புத் தன்மையுள்ள சேய் உட்கருவாக மாறும் அணுக்கரு சிதைவினை ஆல்பாச் சிதைவு என்றழைக்கிறோம்.
- நிலைப்புத் தன்மையற்ற தாய் உட்கருவிலிருந்து பீட்டா துகளை உமிழ்ந்து நிலைப்புத் தன்மையுள்ள சேய் உட்கருவாக மாறும் அணுக்கரு சிதைவினைப் பீட்டாச் சிதைவு என்றழைக்கிறோம்.
- காமா துகள்கள் எனப்படுபவை ஃபோட்டான்களைக் கொண்ட மின்காந்த அலைகளாகும்.
- கனமான அணுக்கருக்கள் பிளவுற்று இரண்டு இலேசான அணுக்கருக்களாக மாறும்போது அதிக அளவு ஆற்றல் வெளியாகும் நிகழ்வு அணுக்கரு பிளவு ஆகும்.
- அணுக்கருப் பிளவின் போது வெளியாகும் சராசரி ஆற்றல் 200 MeV ஆகும்.
- ஒரு சில கதிரியக்கத் தனிமங்கள் பிளவுக்குட்படும் பொருள்களாக மாற்றப்படுகின்றன. இவை வளமைப் பொருள்கள் என்றழைக்கப்படுகின்றன. எ.கா: யுரேனியம் – 238, தோரியம் – 232, புளுட்டோனியம் – 240.
- கட்டுப்படுத்தப்பட்ட அணுக்கரு தொடர்வினையானது அணுக்கரு உலையில் நிலைநிறுத்தப்பட்ட, கட்டுப்படுத்தப்பட்ட முறையில் ஆற்றலை வெளியிடப் பயன்படுகிறது.
- இரண்டு இலேசான அணுக்கருக்கள் ஒன்றிணைந்து கனமான உட்கருக்களாக மாறும் நிகழ்வு அணுக்கரு இணைவு என அழைக்கப்படுகிறது.
- சூரியன் மற்றும் விண்மீன்களில் நடைபெறும் அணுக்கரு இணைவு அல்லது வெப்ப அணுக்கரு இணைவு வினையே ஒளி மற்றும் வெப்ப ஆற்றலின் மூலமாக உள்ளது.
- பாதுகாப்பான கதிர்வீச்சின் அளவு ஒரு வாரத்திற்கு 100 மில்லி ராண்ட்ஜன் ஆகும்.
உங்களுக்குத் தெரியுமா?
- இதுவரையில் 29 கதிரியக்கப்பொருள்கள் கண்டுபிடிக்கப்பட்டுள்ளன. அவற்றில் பெரும் பாலானவை பூமியில் உள்ள அருமண் உலோகங்களாகவும் (rare earth metals), இடைநிலை உலோகங்களாகவும் உள்ளன.
- யுரேனஸ் கோள் பெயரிட்டப் பிறகு அதனைக் கருத்தில் கொண்டு, பிட்ச் பிளண்ட் என்ற கதிரியக்கக் கனிமத்தாதுவிலிருந்து யுரேனியத்தை ஜெர்மன் வேதியியலாளர் மார்ட்டின் கிலாபிராத் கண்டறிந்தார்.
- எலக்ட்ரான் வோல்ட்:
அணுக்கரு இயற்பியலில் சிறிய துகள்களில் ஆற்றலை அளவிடும் அலகு எலக்ட்ரான் வோல்ட் (eV) ஆகும். அதாவது ஒரு வோல்ட் மின்னழுத்தத்தினைப் பயன்படுத்தி முடுக்குவிக்கப்படும் ஓர் எலக்ட்ரானின் ஆற்றலாகும்.
1eV = 1.602 x 10-19 ஜீல்.
1 மில்லியன் எலக்ட்ரான் வோல்ட் = 1 MeV = 106 eV (மெகா எலக்ட்ரான் வோல்ட்)
அணுக்கரு பிளவின் மூலம் வெளியேற்றப்படும் சராசரி ஆற்றல் 200 MeV.
- இரண்டாவது உலகப் போரின்போது ஹிரோஷிமா நகரத்தில் வீசப்பட்ட அணுகுண்டின் பெயர் “Little boy” இது யுரேனியத்தை உள்ளகமாகக் கொண்ட துப்பாக்கியை ஒத்த அணுகுண்டாகும். அதனைத் தொடர்ந்து நாகசாகியில் வீசப்பட்ட அணுகுண்டானது “Fat man” என அழைக்கப்படுகிறது. இதில் வெடிக்கப்பட்ட அணுகுண்டு புளுட்டோனியத்தை உள்ளகமாகக் கொண்டதாகும்.
- இலேசான இரண்டு அணுவின் உட்கருக்கள் இணைவதே அணுக்கரு இணைவு எனப்படும். இதில் உள்ள இரண்டு அணுக்கருக்களும் நேர்மின்சுமைக் கொண்டிருப்பதால் நிலைமின்னியல் கவர்ச்சி விசையின் காரணமாக அவை அருகருகே வரும்போது ஒத்த மின்னூட்டத்திற்கான விலக்குவிசை ஏற்படும். உயர் வெப்பநிலையின் (அதாவது 107 முதல் 109 K என்ற அளவில் மட்டுமே) காரணமாக உருவாகும் அணுக்கருவின் இயக்க ஆற்றலால் இந்த விலக்கு விசையானது தவிர்க்கப்படுகிறது.
- ஒவ்வொரு வினாடியிலும் 620 மில்லியன் மெட்ரிக் டன் ஹைட்ரஜன் அணுக்கரு இணைவு சூரியனில் நடைபெறுகிறது. ஒரு வினாடியில் 3.8 x 1026 ஜீல் ஆற்றல் கதிரியக்கமாக வெளியாகிறது. கதிரியக்கத்தின் செறிவு பூமியை நோக்கி வரும்போது படிப்படியாகக் குறைகிறது. பூமியை அடையும்போது ஒரு வினாடியில், ஓரலகுப் பரப்பில் இதன் மதிப்பு 1.4 கிலோ ஜீல் ஆகும்.
- நமது பூமியின் வயது என்னவென்று தெரியுமா? தோராயமாக 4.54 x 109 ஆண்டுகள் (அதாவது 45 கோடியே 40 இலட்சம் ஆண்டுகள்) அப்படியா?
- அயனியாக்கும் கதிர்வீச்சின் அளவினைக் கண்டறியும் சாதனம் டோசிமீட்டர் ஆகும். அணுமின் நிலையம் அமைந்துள்ள இடங்களில் கதிரியக்கம் வெளியாகும் அளவை அவ்வப்போது கண்டறியவும் மருத்துவ நிழலுரு தொழில்நுட்பத்திலும் பயன்படுகிறது. X மற்றும் காமா (γ) கதிர்கள் வெளியாகும் பகுதிகளில் பணியாற்றுவோர் கையடக்க டோசிமீட்டரை அணிந்து கொள்வதன் மூலம் கதிரியக்க உட்கவர் அளவினை அறிந்து கொள்ள இயலும்.